60年研发黑洞,【GSK VS 辉瑞】谁会杀出重围?
RSV疫苗研发的海量投入,像是“落入了一个巨大的黑洞”。呼吸道合胞病毒(RSV)是一种导致呼吸道感染的常见季节性传染病毒,健康的人体细胞是分散的,而RSV病毒会使人体多个单核细胞聚合在一起,变成巨型的多核细胞,这是婴幼儿下呼吸道感染的首要致病原。→点击查看RSV治疗药物市场格局目前全球唯一获批的RSV感染预防药物是阿斯利康的Synagis(帕利珠单抗),疫苗仍是市场空白,据分析师估计,全球RSV疫苗市场至少达100亿美元。然而RSV疫苗研发是一部屡战屡败的血泪史:辉瑞、Novavax、GSK都曾在这一领域摔倒,因新冠疫苗为人所熟知的Novavax更险些破产。RSV结构谜题 破译“双面”F蛋白 RSV疫苗研发的难点在于其病毒结构,RSV是一种单链RNA病毒,包括8种结构蛋白(F、G、M2-1、M2-2、SH、N、P、L)和 3 种非结构蛋白(NS1、NS2、NS3),其中融合蛋白(fusion protein , F)和粘附蛋白(attachment protein, G)是病毒入侵人体的关键。
G蛋白能与宿主细胞膜受体结合,介导病毒进入宿主细胞内;F蛋白既在病毒进入人体中起到关键作用,又会促进被感染细胞与周围健康细胞之间的合胞体形成。
理论上两者都可以成为疫苗研发的理想靶标,但相对于F蛋白,G蛋白变异较多,相对不稳定,因此F蛋白成为了疫苗开发的重要靶点。
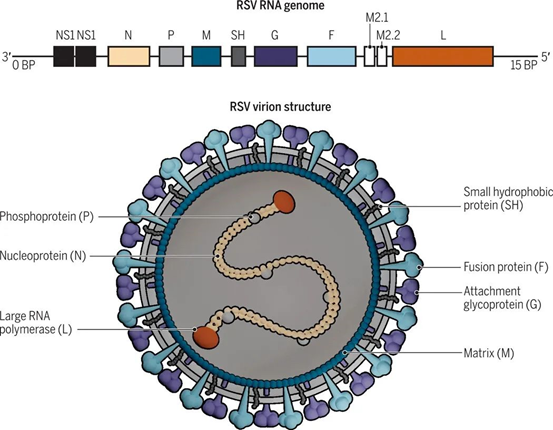
RSV的结构
问题随之而来,F蛋白有两个构相,在感染人体之前,F蛋白处于融合前(pre-F)的亚稳态结构,而在感染人体后,F蛋白又会不可预测地转换为另一种稳定的融合后(post-F)结构。
post-F构象的蛋白,存在着自然保护效果较低的问题,而如果用pre-F蛋白做抗原,稳定性又很难保持。
随着RSV病原学和结构生物学的研究不断深入,科学家们研发了对该蛋白结构进行改造的技术,在增加稳定性的同时也保留了F蛋白pre-F构象的中和敏感性表位,使得pre-F抗原疫苗成为了可能。
辉瑞 vs GSK 并驾齐驱的竞赛
据不完全统计,目前全球已有多款在研RSV产品。从技术路线来看,多种技术同时存在,如减毒灭活疫苗,蛋白亚单位疫苗,病毒载体疫苗,mRNA疫苗等,其中腺病毒载体技术和蛋白亚单位疫苗占据了主体地位。
研发企业方面,以GSK的AReSVi 006与辉瑞的 RSVpreF占据领先地位,二者均在近日发布了积极的三期临床试验结果。
· GSK的老年人呼吸道合胞病毒(RSV)候选疫苗三期数据显示,在关键试验中,严重RSV疾病降低了94.1%,总体疫苗有效性为82.6%· 辉瑞的的老年人呼吸道合胞病毒(RSV)候选疫苗三期数据显示,疫苗效力为85.7%,疫苗耐受性良好,没有安全问题
此外,阿斯利康和赛诺菲也正在开发一种用于婴儿的长效抗体nirsevimab,在3期试验中,RSV相关下呼吸道感染疫苗效力为74.5%。目前辉瑞公司称将在秋季申请批准,GSK更已获得了FDA的优先审查地位,二者极有可能会迎来一场激战。
越来越多的药企涌入RSV赛道,正面交锋只会愈加频繁。

