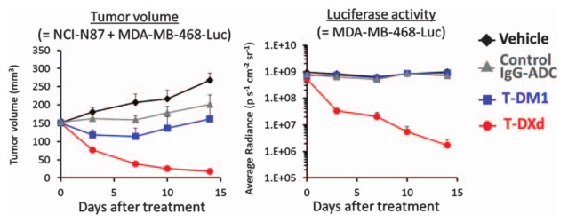
ADC市场发展及有效载荷的开发
01 ADC发展及市场规模
ADC药物在过去十多年间已取得了长足的进展,自2000年第一款药物Mylotarg上市,ADC已历经了三代。
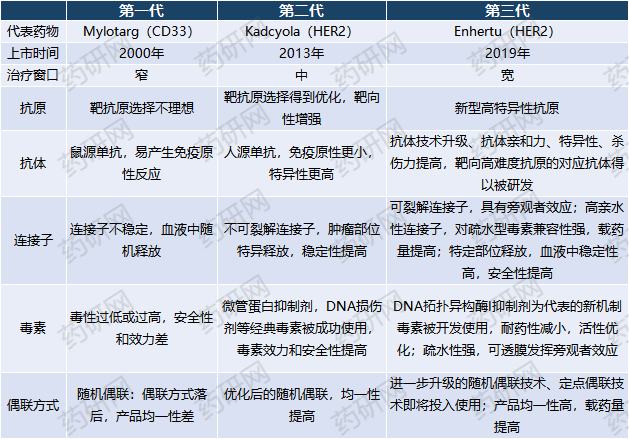
第一代代表药物为Mylotarg,第二代代表药物为2013年上市的Kadcyla,第三代则是2019年上市的Enhertu。在前代基础上对核心组件不断进行迭代优化,使得药物治疗窗口进一步拓宽,疗效也有长足强化:
截止目前,全球ADC药物已上市16款(13款FDA获批,1款国内获批,1款日本获批,1款印度获批),其中11款药物于2019年获批,这些药物带动了ADC的新一轮增长,市场规模逐渐扩增。2021年市场规模约54亿美元,2022年据不完全统计(部分企业年报未公布),市场规模已超76亿美元。
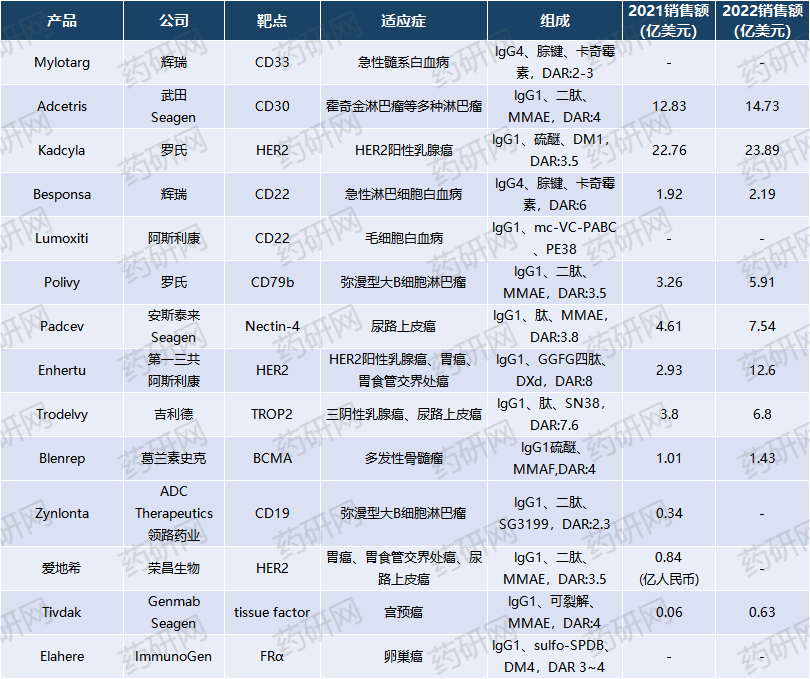
上图为FDA及国内获批的14款药物
02 ADC有效载荷
ADC的组成部分包括抗体、连接子和有效载荷,有效载荷是具有细胞毒性的关键部分。
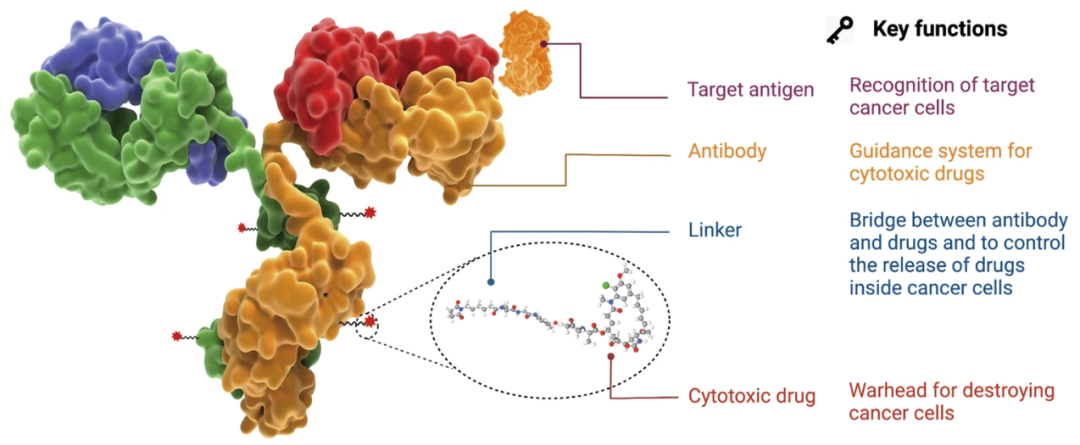
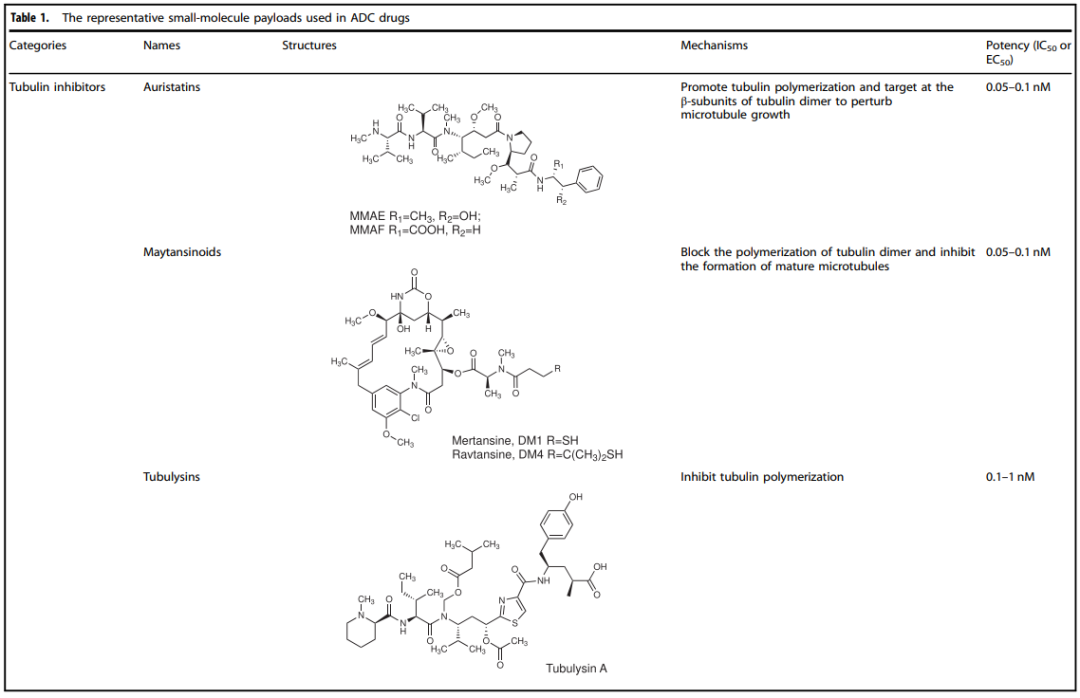
广义上讲,ADC的有效载荷可以是小分子(细胞毒素)、蛋白质毒素、蛋白质、酶和放射性核素。其中有无数的天然或合成的细胞毒素,但只有少数可用于ADC研发。可用作有效载荷的毒素应该是可溶性的,易于结合的,并且稳定。为了引发细胞毒作用,有效载荷应具有某些特性:具有极高的细胞毒效力;目标必须位于细胞内部;分子结构必须体积小,减少免疫原性的风险。根据作用方式,临床试验中的细胞毒素有效载荷可分为三类:微管蛋白抑制剂、DNA损伤药物或转录抑制剂。
微管破坏药物如Auristatins、美登素衍生物(DM1, DM4)、Dolastatins、Tubulysins等微管溶素、Cryptophycins和Eribulin(艾日布林)。
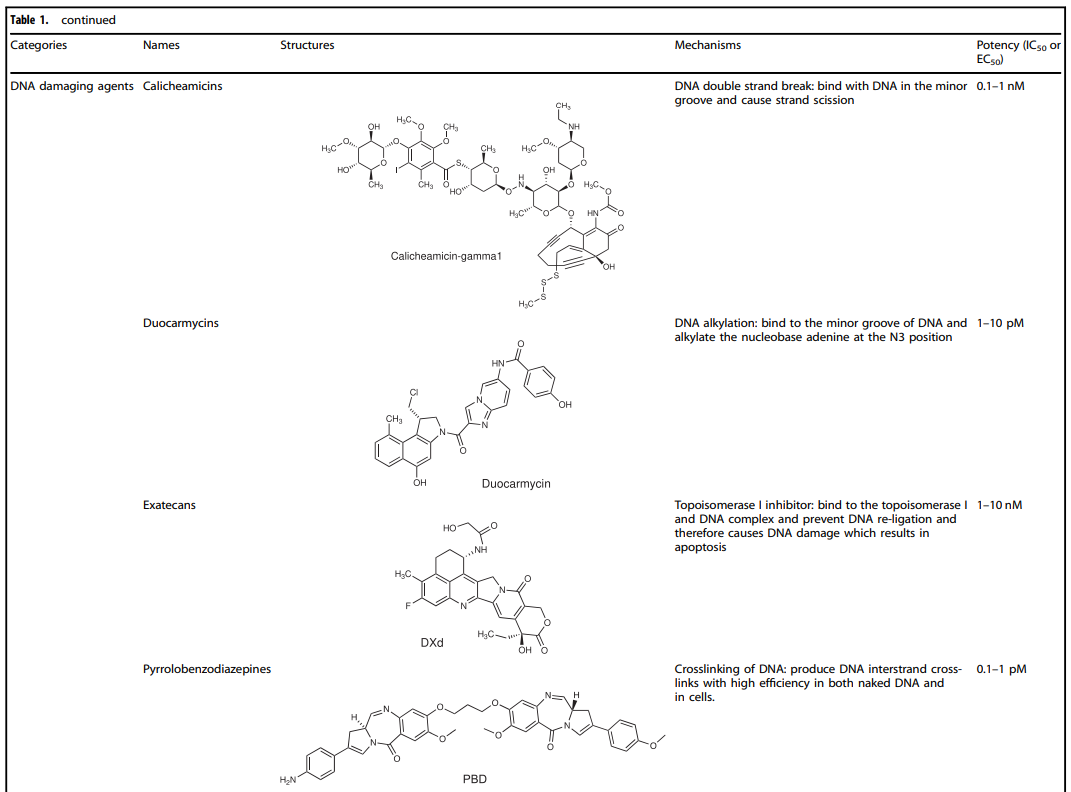
DNA损伤药物:如PBD、卡奇霉素、杜卡霉素、拓扑异构酶I抑制剂。
转录抑制剂如鹅膏毒素 ,α-鹅膏蕈碱是 RNA 聚合酶 II 最有效和特异性的抑制剂,可导致细胞凋亡。
不同的毒素具有不同的效果,如DXd比DM1具有更好的旁观者效应。