当“仅退款”模式开始卷向医药行业
2024年1月11日,复星凯特和国药控股旗下健康管理和患者综合服务平台宸汐健康联合发布了奕凯达(阿基仑赛注射液)中国首款淋巴瘤按疗效价值支付计划。计划推行后,符合条件的患者在使用奕凯达治疗后,若未能达到完全缓解(CR),将获得最高60万元人民币的返还,这是中国首个按疗效价值支付的淋巴瘤药品的创新支付模式,奕凯达也将成为中国首款按疗效价值支付的生物创新药。奕凯达中国首款淋巴瘤按疗效价值支付计划将严格参照《2014版Lugano评估标准》(针对淋巴瘤疗效评估的最新国际权威标准)评估完全缓解(CR)结果。并且,复星凯特将联合包括临床专家、卫健委、治疗示范中心等政府、医疗机构各方共同探讨、建立“治愈”标准。
按疗效付费其实是风险共担的一种模式,也是基于价值定价的一种表现形式,在医药领域,本质是药品购买方和制造方之间对新科研成果的实际疗效和实际付费的协商,旨在让更多患者以更少的顾虑获得最新的治疗技术。
按疗效付费的演变历史
按疗效付费由早期的按绩效付费(Pay for Performance,P4P/PFP)演变而来,最早从英国开始。在英国这种市场准入门槛较高的老牌欧洲国家,国家作为医药唯一购买方,直接为所有医疗服务付费。如果新药没有纳入国家医保体系,药品就无法在临床应用。在二十一世纪之初,药厂需要通过更复杂的卫生技术评估与监管机构谈判,确保自身药品不会被排除在报销系统之外。
谈判的条件千差万别,有的是对特定治疗无效的患者,药厂退还这些患者的全部费用,有的是提供必要的费用以监测患者持续使用特定药品的有效性,并基于实际治疗效果多付或少付。谈判的核心是建立特定治疗的成本效益评判机制。
全球首个常规意义按疗效付费的药物是强生旗下淋巴瘤和骨髓瘤治疗药硼替佐米(商品名:万珂),该药在英国原属于国家医疗服务(NHS)体系报销药,当时全国有2万名此类患者,人均费用1.8万英镑。但万珂只能让70%左右的病人延长2~3年生存期,因此NHS后来将该药从医保中剔除,招致众多患者反对。
后来强生与NHS谈判,采用按疗效付费机制:即当其他治疗无效时,NHS同意使用万珂并支付相关费用,3个月后对患者进行疗效评估,如果评估治疗无效,则立即停止使用,强生退款给NHS。部分按疗效付费案例见表1。
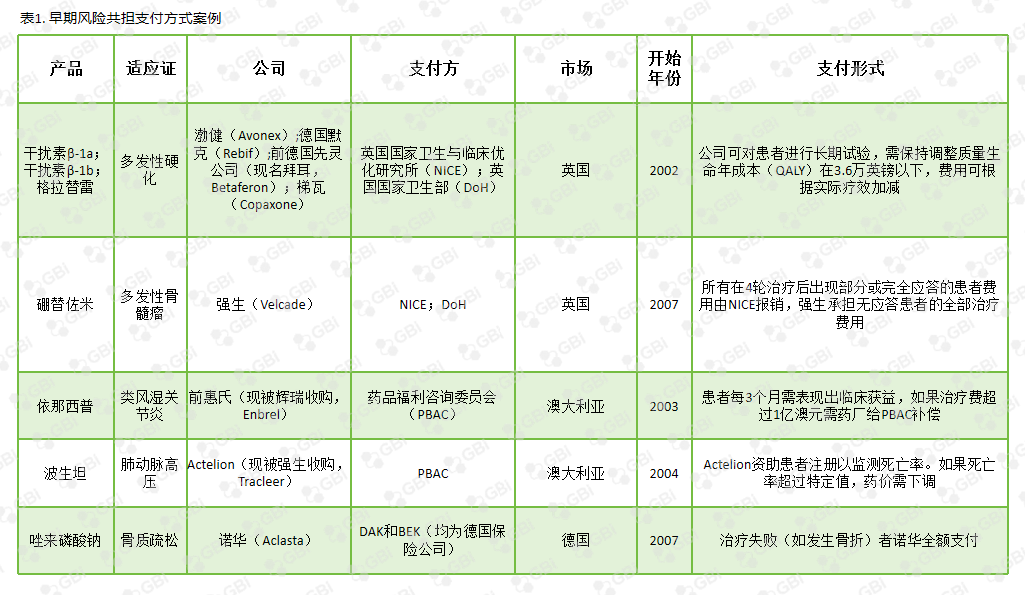
来源:GBI分析
与欧洲市场不同,在美国为劳动年龄人口承保的主要为商业/私人保险,每个险种有各自覆盖的药品清单,保险公司也会通过HTA和效价比分析(CEA)决定保险套餐中要覆盖哪些药品。美国Medicare也会为老年人群承保。与英国(和其他英联邦体系国家)等国家医保会拒绝为高价新药承保不同,在美国不允许因CEA不合适就拒绝创新药。
但是,私人保险在设计保险产品时,还是需要CEA来评估可以纳入哪些产品。目前已有一些药品在美国采用按疗效付费,尤其是高值药品。保险公司和患者需各自支付一部分金额,而且随着药品越贵,患者付费金额也更高,这可能也让患者对选用新疗法有所顾虑。
而对CAR-T这种颠覆传统治疗模式的高端前沿疗法来说,已经显著提高了治疗的潜在成本。CAR-T的定价通常高达40~100万美元/次治疗,主要由于其有望治愈致死性疾病带来的长期潜在效益。但尽管如此,获批上市的CAR-T产品都只有短短几年的临床试验期,尤其那些只做到临床Ⅱ期就附条件批准上市的CAR-T,试验时间就更短。在传统的商业模式下,病人需先付费后获得治疗,而这种新型且昂贵的产品,临床风险如果全部由病人承担明显不公平。
而且,接受CAR-T治疗前后有一系列的准备和善后工作,包括患者预处理、初始化疗、治疗后效果评估、治疗后毒性管理等。在美国市场,上述工作都不纳入CAR-T疗法的支付标准(标价)中,而是由医疗机构实施和负担。因此尽管CAR-T得到医保报销,开展这一疗法的医疗机构可能也会亏损,因为包括住院在内的全套CAR-T治疗费用,比CAR-T本身的费用高出1~2倍。
当然,CAR-T疗法和基因治疗在美国依然可以用传统的商业化模式,但传统惯例已被风险共担支付方式撼动。
以全球最贵的药物——诺华脊髓性肌萎缩症治疗药物Zolgensma (onasemnogene abeparvovec)为例,该药为一次性疗法,如果患者接受治疗后可存活5年,则相当于每年花费42.5万美元。Zolgensma 用于治疗2岁以下的儿童,美国约有1000名这类患者。
诺华子公司AveXis负责该药物的开发和商业化,并与Accredo专业药房(该药房为信诺旗下快捷药方公司PBM业务单元)合作。根据保险公司的赔付计划,Accredo为投保人预先向AveXis支付全部治疗费用后开始治疗,当然可经过协商后进行5年分期付款,后续可根据治疗结果协商折扣。AveXis还可向患者提供可及性和可负担性支持计划。快捷药方公司也希望为其他基因和细胞疗法提供类似支付方案。
在英国和德国,CAR-T疗法Kymriah和Yescarta均获得医保报销,但最终支付的价格取决于真实世界的结果和上市后试验数据。
企业也有不愿意负担的风险
当然,并不是所有的基因和细胞疗法支付方案都进展顺利,尤其是目前一些开发用于罕见病的基因疗法已被搁置一旁。典型的例子是Strimvelis——最早于2016年在欧洲获批的首个体外基因疗法,用于治疗腺苷脱氨酶缺乏症(ADA-SCID)。该疗法由意大利San Raffaele-Telethon基因治疗研究所(SR-TIGET)原研,GSK负责后续开发。
“ ADA-SCID是一种罕见、危及生命的遗传性免疫缺陷,由ADA基因突变引起。该基因可编码产生腺苷脱氨酶,对免疫系统的功能至关重要。由于腺苷脱氨酶缺失,患者免疫系统中的B细胞、T细胞和自然杀伤细胞等细胞功能失常。”
因此,ADA-SCID患者对几乎完全丧失抗病毒、细菌、霉菌的能力,需要长期生活在无菌环境中。ADA-SCID通常在婴儿期就出现感染症状,如果不进行治疗,一般活不过2岁。这种疾病在欧洲仅有15例儿童患者。
尽管该疗法已获批,并以594,000欧元(648,000美元)的价格获得了英国NICE的支持,但由于该疗法只能通过意大利研究中心进行管理,跨境报销流程繁琐,导致从批准治疗到接受治疗需要等待1年的时间。2017年,GSK开始剥离罕见病业务,2018年,Strimvelis被出售给Orchard Therapeutics,然后在2023年7月将营销授权移交给意大利非营利组织Fondazione Telethon基金会,而当初研发该疗法的SR-TIGET正是这个基金会的下设机构。
Bluebird Therapeutics也有两款基因疗法在欧洲市场遭遇了失败:2019年Zynteglo获批用于治疗重度β地中海贫血,定价180万美元;2021年Skysona获批用于治疗脑肾上腺脑白质营养不良,定价300万美元。但由于无法获得报销,这两款产品后来都退出了欧洲市场,转而专注于美国市场。显然,尽管风险共担可以推进患者获得高新疗法,但无法填平开发基因疗法企业的高额研发成本。
参考文献:
1.https://www.baiji.com.cn/news/baiji_news/2017/0816/318908.html;首张“按疗效付费”的保单长啥样?
2.https://mp.weixin.qq.com/s/4NEzGiiCmH-JWJsLHiV03w;全省率先!在攀枝花用传统中医治疗这些病将按疗效付费
3.https://mp.weixin.qq.com/s/WuCVLkF8BQvNadNORWpcAA;浙江试点肝移植术纳入医保,个人自理三成!
4.https://mp.weixin.qq.com/s/s3ta9eukB_gReJ4cI_CTyQ;中医按疗效付费2年带来新变化
5.https://ybj.sh.gov.cn/qtwj/20210414/a4d9d5b7509c4dca99489d6f6fce6e07.html;关于部分诊疗项目试行按绩效支付的通知沪医保医管发〔2021〕14号
6.https://ybj.sh.gov.cn/qtwj/20220120/d85cb2c5f04c44cd8

