中美上市新型冠状病毒检测试剂对比
卫健委公布,3月16日,中国新增确诊病例21例,其中武汉1例,其余新增均为境外输入确诊病例,北京9例,上海3例,广东3例,浙江1例,山东1例,广西1例,云南1例,陕西1例。截至3月16日24时,累计报告境外输入确诊病例143例。
同样的3月16日,海外新增8214例,其中,西班牙新增3438例,意大利新增3233例,伊朗新增1053例,德国新增1174例,法国新增1233例,美国新增913例等,海外累计确诊超过十万例。
两相对比,国外疫情大爆发,我国疫情防控取得了显著效果,疫情防控重点也转向防止境外输入扩散。疫情之下,中国不仅积累了丰富的抗疫经验,更积累了一批检测手段和治疗方法,截止3月16日我国已有17个新型冠状病毒检测试剂生产厂家19个检测产品通过药监局应急审评上市,详情见下表。

医药科技发达的美国,同样通过FDA应急授权上市了一批检测试剂,详情见下表。
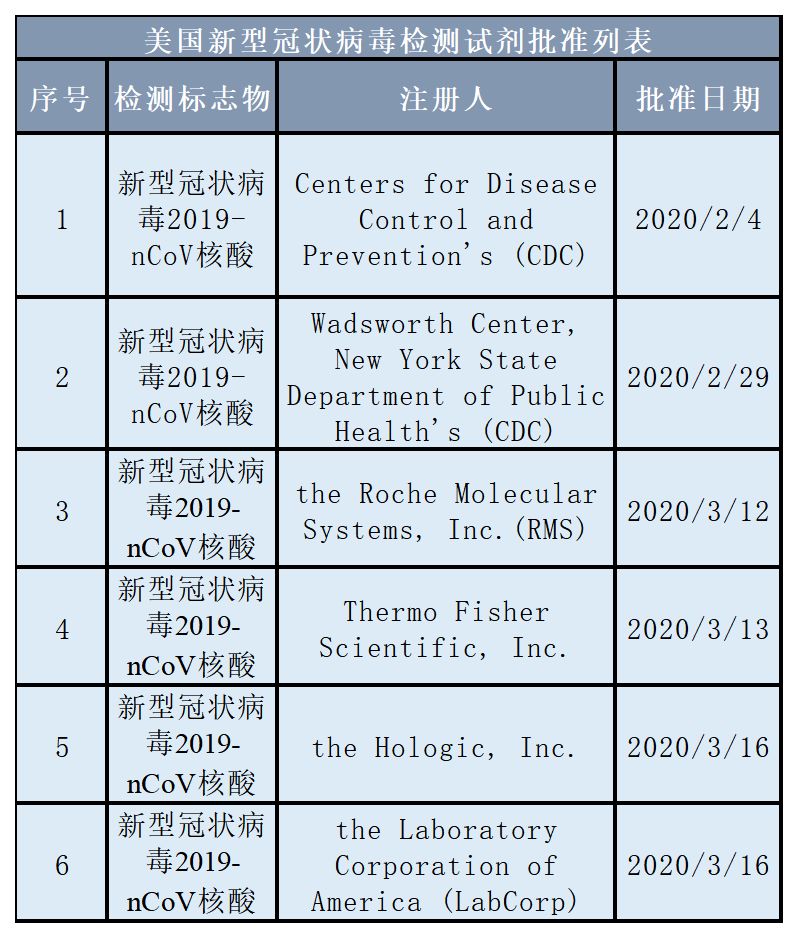
通过对比中美已获批新型冠状病毒检测试剂及其厂家,可发现,中国试剂的生产者全部为企业,而美国在初期仅有美国疾病预防和控制中心(CDC)下属疾病控制和预防中心,在韩国疫情开始爆发后又新增一家,依旧是CDC下属机构,直到3月12日Roche Molecular Systems,(RMS)上市,才有一家企业生产新型冠状病毒检测试剂产品。
中国上市新冠病毒检测试剂包括核酸检测和抗体检测两大类,核酸检测试剂有荧光PCR法、联合探针锚定聚合测序法、恒温扩增芯片法,其中,成都博奥晶芯生物科技有限公司产品可诊断或鉴别诊断者的咽拭子样本中新型冠状病毒(2019-nCoV)S和N靶基因以及甲型流感病毒、新型甲型H1N1流感病毒(2009)、甲型H3N2流感病毒、乙型流感病毒、呼吸道合胞病毒等六种核酸;抗体检测涵盖化学发光微粒子免疫检测法、胶体金法、磁微粒化学发光法等。
截止3月16日,美国已获批6家6个检测试剂,但全部为核酸检测试剂。相对产能与检测试剂种类远低于国内企业,检测场景广度及检测效率亦与过内有较大差距,如此才造成美国检测试剂紧张,入选检测标准高。
虽然,有消息称美国有40余家实验室准备生产新冠病毒检测试剂,但在疫情全球范围迅速爆发的情况下,早一点对密切接触人群进行检查,就可以尽早采取治疗和隔离措施,无论是对于疾病的治疗还是防止扩散传播,都非常重要。
据悉,厦门万泰凯瑞生物技术有限公司,3月内月产能将超100万人份,厦门万泰母公司北京万泰2月26日就已向韩国紧急出口了一万人份的酶联免疫法新型冠状病毒抗体检测试剂,万泰生物相关新冠病毒检测试剂也获得欧盟准入。达安基因3月3日新型冠状病毒核酸检测试剂盒已获得欧盟CE认证。2月4日,华大基因公司表示,该公司已经完成了约30万人份的新型冠状病毒检测试剂盒生产,日均产能已达到8万人份/天。同时已继续紧急安排增加生产30万人份试剂盒,新储备30万人份试剂盒的原料。
综上所述,相比美国,中国的新型冠状病毒检测试剂,种类齐全,产能充足,经过了在国内的应用检验,检测场景广度大,检测效率高。在中国新增感染人群迅速下降的现在,国内的新冠病毒检测试剂厂商产能未减,且大部分保质期为6个月,如果政府能够帮助国内企业迅速对接疫情爆发的国家,如:意大利、德国、西班牙、英国等,其一,可帮助这些国家防控疫情,彰显负责任大国的形象;其二,毕竟,新冠病毒检测试剂厂家虽然在国内做出了贡献,但获利并不大,实现对外出口,不仅增加厂家利润,还可帮助国内企业扩大国际知名度、打开国际市场。

