瑞德西韦(remdesivir)无需美国授权,但抗击2019-nCoV仍需努力
在双黄连结束神奇的抢购潮后,小分子抗病毒药瑞德西韦(remdesivir)再次给国人带来希望。1月31日,权威医学杂志《新英格兰医学杂志》(英文名:The NEW ENGLAND JOURNAL of MEDICINE, NEJM)在线文章《First Case of 2019 Novel Coronavirus in the United States》公布美国首例患者在接受单一抗病毒药——瑞德西韦治疗(接受其他治疗为抗生素及维持治疗)后痊愈, 2月2日原研公司吉列德(Gilead)表示与北京中日友好医院将合作开展三期临床,预计招募270位患者并于4月27日结束临床研究。
让人无语的是网络上突然红火的“特朗普特批豁免瑞德西韦对中国的专利”,还有“向中国紧急公开药物分子结构至4月27日“,这是得有多外行?
首先,药物自其进入临床研究就需要公开其分子结构,瑞德西韦已经结束了临床二期,适应症埃博拉病毒感染,证明其安全性和对冠状病毒感染疾病的有效性。其次,虽然吉列德在中国申请了瑞德西韦的化合物专利,但是根据国际贸易协议《多哈宣言》、《中华人民共和国专利法》等政策、法规,在遭受危害公众健康危机时,受灾国有权对该药品进行强行仿制,即无论原研公司吉列德授权与否,中国都可以授权国内药企强行进行仿制。
问题的关键是目前尚无国内企业完成瑞德西韦化学合成及制剂工艺的全流程研究,即国内企业不具备瑞德西韦的生产能力,靠国内药企生产需要耗费较长的研发时间,而疫情不等人,如果想获得质量可靠的瑞德西韦只能与吉列德合作,首先,验证瑞德西韦在放大样本量的情况下依然疗效确切,然后,在2019-nCoV患者中全面开展标准治疗。
与瑞德西韦共同靶点——RNA-dependent RNA polymerase(RdRP,RNA依赖性RNA聚合酶)的法匹拉韦,在日本已经上市用于治疗流感,同适应症在美国已完成3期临床,临床显示,治疗流感效果强于奥司他韦。与利巴韦林(英语:Ribavirin,俗称病毒唑)联合治愈两名拉沙热(RNA病毒拉萨热病毒引起的疾病)患者。在治疗埃博拉病毒感染中,法匹拉韦对低病毒载量的患者效果较佳,但对高病毒载量的患者效果较差。2月2日,已治愈多名新型冠状病毒感染者的深圳市第三人民医院(国家感染性疾病临床医学研究中心)将其列入本院的“新型冠状病毒肺炎诊疗方案“。与瑞德西韦不同的,法匹拉韦化合物专利已于2019年到期,国内多家企业曾进行仿制,如下图所示:
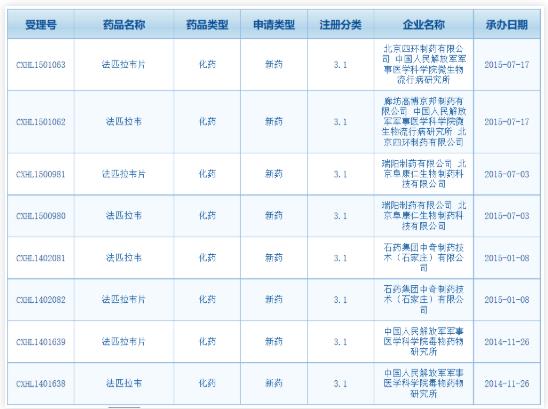
因国内药品研发政策变化,大部分企业放弃继续研发法匹拉韦,最终仅中国人民解放军军事医学科学院毒物药物研究所与海正药业合作,坚持按照新的政策要求继续研发,法匹拉韦进入仿制药临床阶段,目前,海正药业具备生产法匹拉韦的能力。2月3日,海正药业公告已向药监局提交生产申请。
洛匹那韦/利托那韦作为抗艾滋病药物,在国家卫生健康委《新型冠状病毒感染的肺炎诊疗方案》试行第三版和第四版中均做为主要推荐药物,2月2日泰国曼谷拉察威提(Rajavithi)医院的肺部疾病专家Kriangsak Atipornwanich表示洛匹那韦( lopinavir )和利托那韦(ritonavir)的混合药物,联合大剂量的流感药物奥司他韦(oseltamivir),该组合疗法对两位新冠肺炎患者有显著效果,其中一名为重症患者。目前,国内上市产品为雅培进口洛匹那韦利托那韦复方片剂及口服溶液,另歌礼药业已完成利托那韦单药的BE研究。
值得注意的是,《新型冠状病毒感染的肺炎诊疗方案》试行第四版“重型、危重型病例的治疗“中删除了血必净注射液,其原因可能是中药注射剂毒副作用较大。虽然如此,2月3日,血必净注射液的生产企业,天津红日药业依然盘中封涨停了。
以上几种可及性较高的抗病毒药物中,瑞德西韦最有抗新型冠状病毒的潜力,海正药业虽已向药监局提交生产申请,但适应症仅为流感,未来能否真正被广泛应用于治疗新型冠状病毒相较瑞德西韦尚有较大的不确定性。洛匹那韦利托那韦复方片也仍需要进一步验证其疗效。
综上,药品研发上市是一个系统而复杂的科学研究过程,现代医学不仅是治病,更要降低毒副作用及治疗后遗症,从现有可及的药物中快速筛选出有效治疗新型冠状病毒感染的药物,确定效果明确的治疗方案,对阻止疫情恐慌的蔓延至关重要。

