转战罕见病领域,国内企业能承受得住吗?
罕见病发病率低、患者群体小。
我国医药企业选择性“忽视”该领域药物的开发,主要原因还是疾病的发病率在十万甚至百万分之几水平,市场规模小,且药物研发风险大,企业无利可图。相比较来看,企业更热衷于消化系统、内分泌系统、肿瘤等有更大患者群体的药物研发,不过同时也造成了部分疾病领域赛道拥挤,产品同质化现象严重。
因此,在现阶段激烈的市场竞争环境下,企业都在积极探索升级转型之路,寻求未来新业务的增长点。小编在医药领域还有景气之地,你打算怎么选?一文中提到,产品立项是未来医药企业的竞争点,唯有提供具有临床价值的产品(填补临床用药空白或降低用药负担),企业方能在市场中获益。目前来看,我国孤儿药市场尚处于待开发阶段,未来蕴藏着巨大价值。
在我国《第一批罕见病目录》中,绝大多数疾病仍无药可用。中国上市且有罕见病适应症的药物仅涉及30余种疾病,并且我国罕见病创新治疗药物基本被国外企业垄断,国内企业创新品种处于空白;同时,国内仿制药缺位,也基本处于待开发领域。
以“常见”罕见病——特发性肺动脉高压为例,国外已有11种(以通用名计)治疗药物,其中7个品种在我国进口上市,直到2018年国内才有安立生坦仿制药上市。
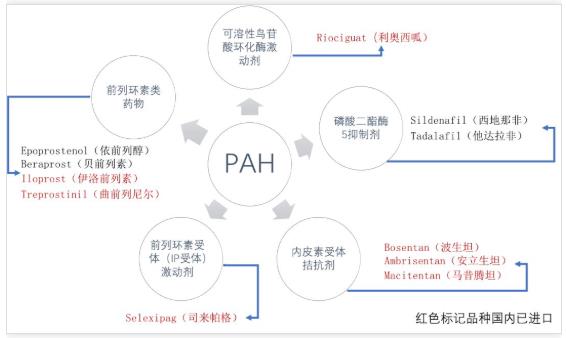
值得注意的是,磷酸二酯酶抑制剂他达拉非、西地那非药物在我国上市多年,专利期已过,而肺动脉高压适应症至今未在我国上市。但《罕见病诊疗指南(2019年版)》中指出,由于这些药物疗效可靠、价格便宜,已成为我国肺动脉高压的一线治疗药物。对于这类临床超适应症用药普遍、但适应症尚无注册获批的罕见病药物来说,产品市场小、临床试验开展困难、竞品压力大或是企业未在我国注册申报的一个重要原因。
根据艾美达样本公立医院数据显示,2018年肺动脉高压靶向治疗用药整体市场规模近三千万元,波生坦一直是临床主要用药。2019年前三季度,国内安立生坦的仿制药销售份额将近原研品种的七分之一,这对于上市仅一年的仿制品种来说,未来还是有一定市场空间的。不过,国家推行仿制药带量采购以来,药品降价幅度有目共睹。罕见病用药价格高,随着集采范围扩大,未来罕见病用药面临集采降价也是发展趋势。然而大部分罕见病用药不同其他常规用药领域,即便全国带量,市场空间仍可能狭窄。如若同样纳入集采范围,一边是压缩价格,而另一边销量却无法大幅增长,想必企业的积极性会受到不小打击吧。所以说,罕见病用药的集采工作应谨慎考虑,区别对待。
再比如罕见病中的“大病种”——血友病。我国血友病临床用药以血源性凝血因子(国产)和重组凝血因子(进口)为主,长效重组凝血因子至今未在国内上市。由于该类药物研制的技术含量高, 国内获批生产的企业品种均为血源性凝血因子。得益于近两年药政改革,2018年获批进口的非凝血因子疗法艾美赛珠单抗是目前我国唯一治疗血友病的长效制剂。
可以看出,不论是特发性肺动脉高压用药,还是血友病药物,我国企业在创新药、仿制药研发方面均有待加强。各项利好政策接踵而至,国内患者用药问题得到显著改善,而国内医药企业在药物开发方则依然面临诸多压力和挑战:如政策不完善,基础研究薄弱、缺乏核心技术,病例稀少、招募困难、试验主要疗效终点的选择困难等临床研究挑战。
因此,对于国内致力于罕见病药物研发的企业来说,敢于争做“第一批吃螃蟹的人”,就要主动参与推动我国罕见病相关政策的建立和完善,抢占先机。同时要做好企业定位,选择适合自身发展的道路:仿制药开发?创新引进?还是自主研发?无论哪一种情况,最终目标就是要能够提供有临床价值的产品。或提供当前完全未被满足的临床需求,创造全球first-in-class,填补临床用药空白;或提供当前治疗方案中可替代品种,降低用药负担。即在Me-too/better类药物开发方面,企业品种前景体现在价格优势或疗效优势。企业只有在罕见病药物研发中做出更长期、更稳定的经济投入,才能真正为我国罕见病患者带来更多有效的药物。
国际市场上,孤儿药市场热度高居不下。据《Orphan Drug Report 2019》报告指出,全球孤儿药市场2018年有1310亿美元的销售额,预计到2024年达到2420亿美元。国际大型制药企业在罕见病布局方面逐步形成了自己的优势领域。而较于国际市场,我国孤儿药市场仍处在边缘境地。随着我国罕见病政策红利持续释放,参考全球孤儿药市场预测,未来中国孤儿药市场释放空间可观,潜力可期。
新品速递
《中国罕见病行业研究报告》报告完整目录如下:


