【盘点】通过优先审评审批获CFDA批准上市的化药品种
2016年2月CFDA发布了《关于解决药品注册申请积压实行优先审评审批的意见》。加快具有临床价值的新药和临床急需仿制药的研发上市,明确了优先审评审批的范围及程序。
纳入优先审评的品种理由主要有:与现有治疗手段相比具有明显治疗优势;丙型肝炎、乙型肝炎及艾滋病治疗药物;儿童用药品、罕见病等临床急需品种;首仿品种;针对同一生产线上,已在欧盟、美国上市品种。
根据CDE公开数据显示,截止到2017年11月30日,已纳入优先审评审批的品种涉及受理号有383条。按通用名计算,涉及品种共有192个:其中,化学药156个,生物制品32个,中药4个。
在纳入优先审评审批的化药品种中,目前已获CFDA批准上市的共42个,详见下表。
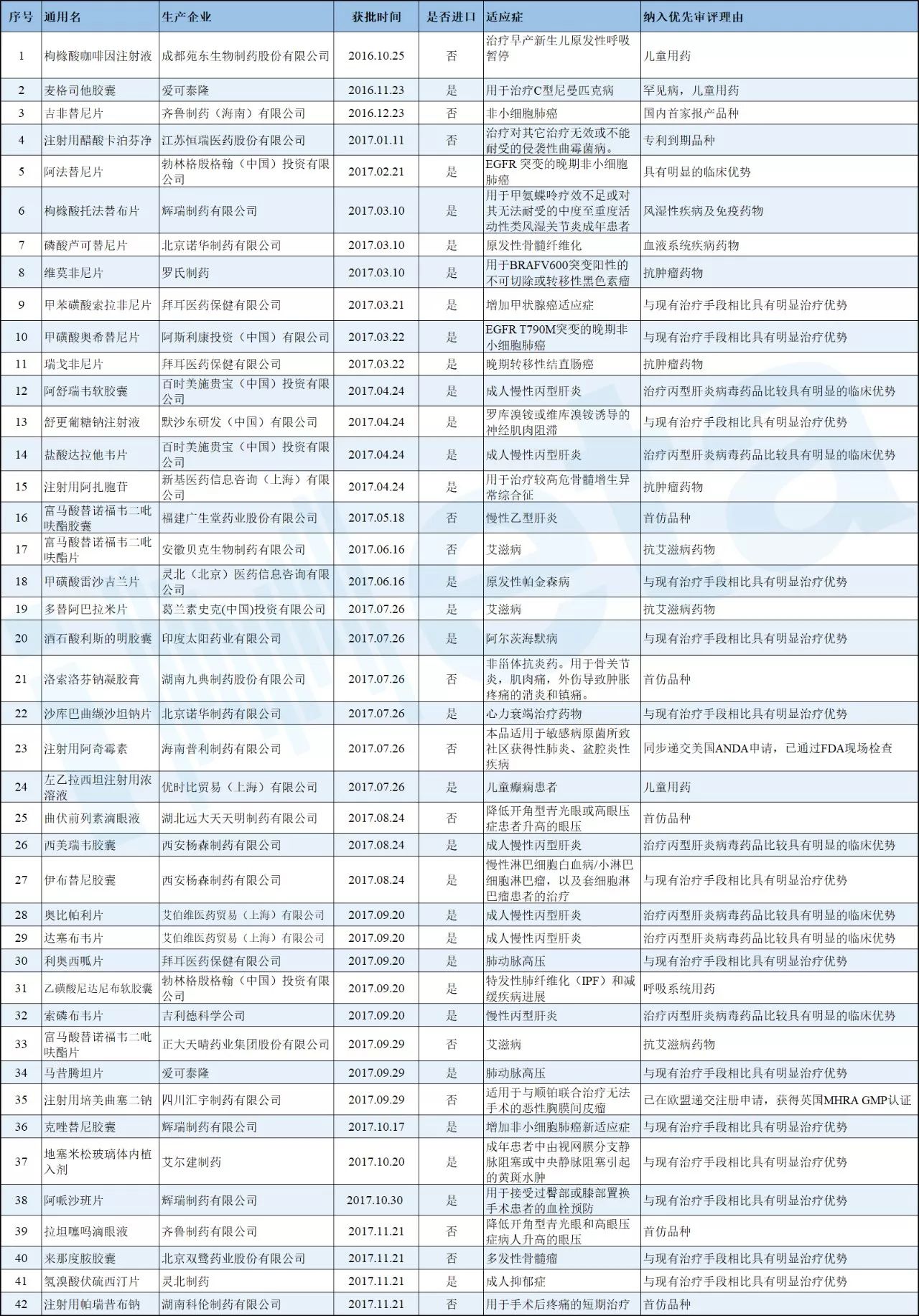
数据统计截止时间2017.11.30;CFDA已有批准文号。

