在“钱窝”里孵化的新药,能换得“金蛋”吗?
近些年,医药圈内的热钱就像雨后春笋般喷涌而出,一次又一次的刷新着融资金额上线。前有互联网+医疗,后有创新药企业,其中信达生物以17亿元刷新了国内生物医药领域最大一笔融资。所谓能力越大责任越大,融得的这些钱要最终换成产品在市场中大卖,投资者才会继续投钱,从而形成良性循环。本期,小编带领各位来盘点下,近些年获得融资企业的在研产品,现在如何了?谁将决定未来市场?
筛选依据:2015~2017年,国内获得融资金额TOP5的企业,已提交临床申请的1类新药。
信达 2016年 D轮融资17亿元
重组全人源抗前蛋白转化酶枯草溶菌素9(PCSK-9)单克隆抗体注射液,降脂,2017/2/13 提交临床申请,目前在审评审批中。
重组人血管内皮生长因子受体-抗体-人补体受体1融合蛋白注射液,研发代码:IBI302,多种眼底黄斑疾病和实体瘤,2015/4/21提交临床申请,2016/12/22制证完毕已发批件。
重组全人源抗前蛋白转化酶枯草溶菌素9(PCSK-9)单克隆抗体注射液
PCSK9单抗前蛋白转化酶枯草溶菌素9是立普妥之后最热的降脂靶点。全球目前仅上市了2个PCSK9单抗药物,分别是安进的Repatha和赛诺菲/再生元的Praluent。但是,Repatha和Praluent月均治疗费用在1400~1500美金左右,患者用药负担相当大!而立普妥在国内月均用药负担在四百元左右。
由于生物制品与传统上的固体制剂不同,在保存运输以及使用方面相对普通制剂条件更为苛刻,最终体现在患者手中时,便是每次用药需到医疗机构方可使用,而这成为了患者用药的“最后一公里”。
从目前已经获批的两个PCSK9抑制剂来看,批准的使用患者,仅限于那些他汀类药物无法控制胆固醇水平的患者,或因遗传疾病导致胆固醇水平过高的患者。因此,对于他汀类而言,暂时市场还不会被大幅侵占。
由于Repatha和Praluent价格昂贵,上市后市场销售并不理想,有业内数据显示,两个药物在2016年全球销售额在1亿多美元,未来是否放量,不好说。立普妥在1996年上市后,一直到2006年达到销售峰值,高达128.86亿美元。
有时候物以稀为贵,但是在医疗圈里,光贵是不行的,还要亲民才可打开市场。信达生物在研的PCSK9是否会突破Repatha和Praluent的销量情况,最重要的便是药物适用范围和价格了;对于价格来说,药虽好,但买不起,未来的路会很艰辛。
从用药负担、使用方式、临床疗效以及价格方面综合考虑,PCSK9能否成为下一个“立普妥”,虽然它很热,但是小编还是压“小”吧。
重组人血管内皮生长因子受体-抗体-人补体受体1融合蛋白注射液
有资料显示,其用于治疗多种眼底黄斑疾病和实体瘤,其中眼底病为年龄相关性黄斑变性(AMD),给药途径为玻璃体内注射。目前,市场中治疗AMD的药物有康柏西普和雷珠单抗,均为眼底注射。
有意思的是,康柏西普的主要研发者之一是信达公司的老大--俞德超,这背后是有故事的,等有机会小编再带领大家深挖八卦~
康柏西普于2014年上市,在上市后便与雷珠单抗争抢市场份额。在艾美达全国样本公立医院数据库中,康柏西普在2016年购药总额为1.69亿元,复合增长率高达161.0%,对比雷珠单抗购药总金额,2016年为3.21亿元,复合增长率为10.6%,并且雷珠单抗2016年购药总金额与2015年持平。由此可见,康柏西普对雷珠单抗的冲击非常之大。
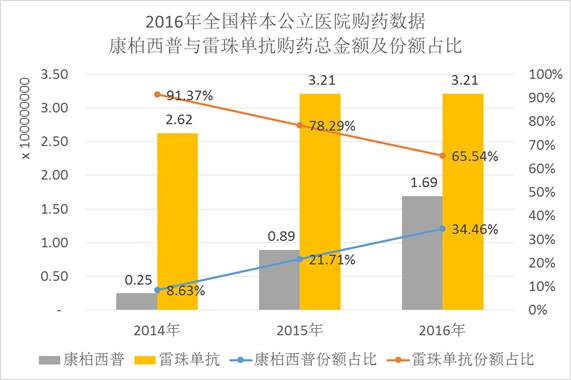
俞老大作为康柏西普的主要研发人,清楚的知道其中的故事,本次研发IBI302,相信将对康柏西普和雷珠单抗造成巨大影响。小编这次赌“大”~
歌礼 2017年 B轮 融资1亿美元
ASC16片,丙肝,2015/4/30提交临床申请,2016/5/19制证完毕已发批件
丹诺瑞韦钠片,丙肝,2017/1/3提交上市申请,目前在审评审批中
ASC16片于2015年提交临床申请,丹诺瑞韦钠片于2017年提交上市申请,均用于治疗丙肝的口服物。其中丹诺瑞韦临床的三联方案治疗中国基因 I 型丙肝患者 12 周,治愈率超过95%。丹诺瑞韦钠在2014年初首次申请临床,在2017年便开始申报上市生产,研发速度令人惊叹,是本次统计时间内唯一一个上市申请的1类新药。
目前该药物进入优先审评,有望成为国内企业第一个获批上市的丙肝治疗药物。但是,进口药品已有丙肝治疗药物获得CFDA批准上市,为BMS的盐酸达拉他韦片和阿舒瑞韦软胶囊联合治疗慢性丙肝,据悉还有一款强生西美瑞韦已获得CFDA批准上市,尚未公布药品批准文号。
目前治疗丙肝的方法主要有两种,一种是聚乙二醇干扰素合并利巴韦林,疗程持续一至两年。但是近一半的患者不耐受干扰素,会出现骨髓抑制和溶血、肾脏损害、精神异常等副作用,而适用干扰素的患者也仅有60%左右能被治愈。
另一种是口服小分子抗病毒药物,疗程仅12周,治愈率达90%以上,且适用干扰素不耐受人群,在欧美已成为主流治疗方法。但这一领域被国际药业巨头垄断且价格昂贵。
值得引起注意的是,ASC16片临床申请和丹诺瑞韦钠片上市申请均已被纳入优先审评名单中,前者已制证完毕已发批件,后者在审批审评中。在历次纳入优先审评名单中,便有十余种丙肝抗病毒药物,其中就有重磅药吉利德的索磷布韦片;虽然市场中治疗丙肝药物屈指可数,但争抢上市的药物却越来越多,未来竞争将会非常激烈。
丙肝药物市场巨大,但是如此多的药物集中在同一时段上市,竞争激烈程度将惨不忍睹,在进口药已获得批准文号的前提下,丹诺瑞韦钠片的压力不言而喻。若没有足够的临床优势,价格战或成为抢占市场的必经之路,不知已上市的进口药品定价如何。如果按照进口药品定价传统惯例,患者用药负担不会轻松,这或许是丹诺瑞韦钠片的赶超机会。
再鼎 2016年 B轮融资1亿美元
ZL-2302片/胶囊,非小细胞肺癌(NSCLC),2017/4/27提交临床申请,目前在审评审批中
ZL-2303片,非小细胞肺癌(NSCLC),2016/5/13提交临床申请,目前在审评审批中
ZL2301/丙氨酸布立尼布片,肝细胞癌,2016/7/15 提交临床申请,2017/3/7制证完毕已发批件
ZL-2306胶囊,乳腺癌、卵巢癌,2017/3/1 提交临床申请,目前在审评审批中
ZL-2102胶囊为PGD2合成酶抑制剂,慢性呼吸性疾病(哮喘和慢性阻塞性肺炎),2015/8/24提交临床申请,2017/4/17制证完毕已发批件
再鼎医药在研产品线较为丰富,以上产品均为临床申请,以癌症为主攻方向,其中非小细胞肺癌有ZL-2302和ZL-2303。目前,非小细胞肺癌治疗药物有吉非替尼、厄洛替尼、埃克替尼、克唑替尼、奥希替尼、阿法替尼等多个产品。
当然,每个产品有不同的细分适应症,如果现有产品无法让各位产生紧张之感,辣么,小编要放出来非小细胞肺癌在研项目了。截止到2017年5月底,国内治疗非小细胞肺癌靶向药物临床试验公示品种共有26个;截止到2017年6月20日,CDE申请进口药品24个品种,新药23个品种。除去重复品种,共有63个通用名药品正在走向市场。有木有被吓到了?在逐渐成熟的NSCLC靶向治疗药物中,想要杀出一片市场,强大的临床优势是必要条件,此外,价格因素也是决定其市场份额的重要因素。
目前,我国市场中竞争最激烈的靶向药物适应症非NSCLC莫属,虽然的上市产品屈指可数,但是奔向市场的产品加上脚趾头也数不过来。当然极高的发病率是造成这一现象的主要原因,不过蛋糕越大竞争者也就越多,最后能抢占的份额也就越来越少。相反,那些看似发病率不那么高的适应症领域,因为鲜有人问津,有更大的市场潜力,比如:我国发病率和死亡率较高的胃癌、肝癌、结直肠癌和食道癌,女性乳腺癌和卵巢癌等。
相比治疗NSCLC的药物来说,小编倒是更看好丙氨酸布立尼布片和ZL-2306胶囊。目前,治疗肝癌的小分子靶向药物仅有索拉菲尼在我国上市,2016年CDE申请也仅有2个小分子靶向治疗药物。治疗乳腺癌的小分子靶向药物仅有拉帕替尼在我国上市,但是,2016年CDE申请有8个小分子靶向治疗药物。
由此可见,企业已经发现门路了,乳腺癌小分子靶向治疗药物极有可能成为下一个NSCLC,谁能首先快速上市直接决定了抢占蛋糕的大小。
百济神州 2015年 B轮融资9700万美元
BGB-A317注射液,PD-1抗体,2015/11/11提交临床申请,2016/9/3制证完毕已发批件
BGB-290胶囊,黑色素瘤、卵巢癌等多种癌症,2015/11/1提交临床申请,2016/8/12制证完毕已发批件
BGB-283胶囊,黑色素瘤、卵巢癌等多种癌症,2014/5/20提交临床申请,2015/7/27制证完毕已发批件
BGB-3111胶囊,多种类型的淋巴瘤,2015/2/13提交临床申请,2016/3/11制证完毕已发批件
注射用Intetumumab单抗,实体瘤,2012/11/12提交临床申请,2014/7/31制证完毕已发批件
BGB-A317注射液
近期最火的没有之一PD-1,在国内外掀起了研究热潮,PD-1/PD-L1抗体虽然还没有产品在国内正式上市,但目前在临床试验阶段的已有8家国内本土企业,据业内统计,国内在研或在登记阶段的已超过30家药企。与传统靶向药物不同,PD-1的适应症较为广泛,目前FDA批准的肿瘤类型有黑色素瘤、非小细胞肺癌、肾癌、头颈癌、膀胱癌和结直肠癌,所以众多企业纷纷投向PD系列的怀抱。(PD-1/PD-L1抗体:五雄并起,细数“诸侯”各家)
PD系列是不是好用,需要市场的验证,能不能获得大卖还需要医生和患者的肯定。但是,挡在前面的一条鸿沟是能不能顺利做完临床并上市;同时,在国内还面临着众多研发企业的竞争,未来的路不一定好走啊!
BGB-290胶囊、BGB-283胶囊、BGB-3111胶囊
对于百济神州其他抗肿瘤胶囊产品来说,小编先带领大家看一看所涉及到的适应症靶向药情况。
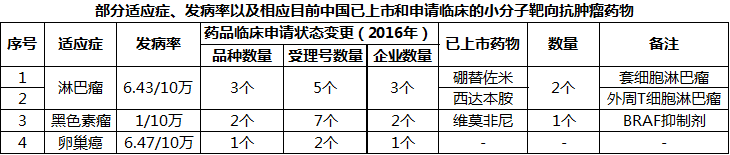
可以看出来,相对火热的非小细胞肺癌靶向治疗药物,百济神州在研品种更偏向“小众”的肿瘤适应症。市场中需要的便是这些看似“无人问津”的肿瘤药,临床需求尚未被满足,尤其是卵巢癌,目前国内没有上市品种,市场空间巨大。
有资料显示,BGB-290胶囊、BGB-283胶囊、BGB-3111胶囊均已在澳大利亚完成了一期临床。临床结果显示,这3个药物分别对黑色素瘤、卵巢癌、淋巴肿瘤等多种癌症疗效显著,而且副作用很小,明显优于同类其他药物。
最终如何,让我们拭目以待吧!
华领医药 2016年 C轮 融资5000万美元
HMS5552片,II型糖尿病,2012/11/28提交临床申请,2013/8/22制证完毕已发批件
HMS5552片是由华领医药研发的葡萄糖激酶激活剂,是一类全新机制新结构小分子口服糖尿病药物,想要了解HMS5552片的II期临床试验结果,请点击:糖尿病原创新药HMS5552公布单药治疗II期临床试验结果,数据来源:第一届“中国医药创新与投资大会”全球临床数据首发-创新药在中国医药创新与投资大会全球临床数据首发上亮相。
在艾美达全国样本公立医院数据库中,ATC2分类中糖尿病治疗药物在2016年购药总金额为68亿元左右,购药总金额TOP10如下图所示。可以看出,目前市场中常见降糖药物均为“老药”,例如:阿卡波糖、二甲双胍。
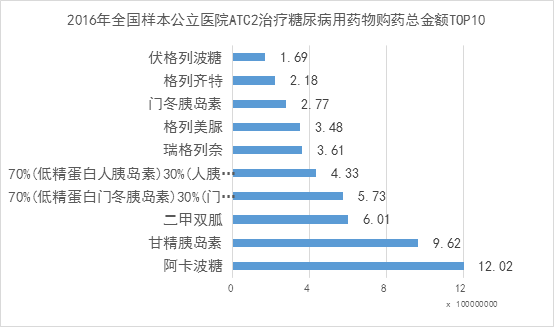
可以说,糖尿病用药市场已然非常成熟,想要在这个市场中杀出一片天地,强大的临床优势是必要条件;从另一方面,在成熟的市场中,价格因素也将成为决定其成败的关键。感兴趣的小伙伴可以好好研究下HMS5552的II期临床数据,看看是不是有不一样的竞争优势。
长风药业 2017年 D轮 融资4.4亿元
在盘点过程中意外出现一匹黑马,小编发现长风药业在近期刚刚完成4.4亿元D轮融资,但在CDE审评审批清单中,却只有一个5.2类和3.2类药品申请,尚未有成熟产品在国内上市。其比较有特色的地方是专注于吸入制剂的研究,治疗领域包含哮喘,慢性阻塞性肺病和鼻炎,在吸入制剂细分领域中有较强优势,吸入制剂的研发生产均有极高的要求。
小编好像有些明白为什么长风药业在尚无产品上市,且 CDE公开的受理品种目录中,无1类新药申请信息的情况下,仍能获得4.4亿元的融资。在艾美达全国样本公立医院数据库中,2016年呼吸系统购药总金额显示,吸入剂型共有22个通用名药品,占据了30%的市场份额,而其他剂型共有178个通用名药品,占据了70%的份额。也就是说,11%的药品占据了市场30%的份额,由此可见,呼吸系统吸入型用药市场潜力巨大。
随着创新发展与资本投资愈来愈紧密的相连,医药或将成为投资领域的常青藤。对于企业来说,自家新药都如同怀胎十月生养长大的孩子,希望能在研发上市过程中给予更多的投入和机会,而这就需要足够的资金支持。在本次盘点中,五家研发企业有四家参加了首届“中国医药创新与投资大会”,分别进行了全球临床数据首发和企业路演等项目,获得了广泛的关注。小编不敢说他们的融资归功于参加了“中国医药创新与投资大会”,但是可以肯定:参加了本届会议,使得其知名度更高,为融资增加了谈判筹码。
对于投资来说,在会议中可以获得国内最最最最前沿的医药研究情况,并且可以与企业进行直接交流,为下一步投资计划奠定坚实的基础。一句话,好项目哪里找?第二届“中国医药创新与投资大会”这里找!
并且,在第二届“中国医药创新与投资大会”中,新增加了医疗器械领域,心动的小伙伴们千万不要错过一年一度的医药创新投资圈盛世!

