那些年,FDA批准的中国仿制药
根据总局关于落实《国务院办公厅关于开展仿制药质量和疗效一致性评价的意见》有关事项的公告,“在中国境内用同一条生产线生产上市并在欧盟、美国或日本获准上市的药品,受理后一致性评价办公室通知药审中心对原境内、外上市申报资料进行审核,通知审核查验中心对生产现场进行检查。经审核批准视同通过一致性评价。”这意味着在欧、美、日上市的药品生产企业,可以免去购买参比制剂、争抢BE资源的烦恼,从而在一致性评价中抢得先机,赢在起跑线。小编近日统计了国内目前在美国上市的仿制药品种和厂家,供大家参考。
此次统计为不完全统计,以国内企业在美国获得ANDA文号为标准,共涉及16个企业的80个品种(包括部分已退市产品),欢迎大家进行补充和探讨。生产相同品种口服固体制剂仿制药的企业要打起一百分的精神了,国家局曾有文:“第一家品种通过一致性评价后,三年后不再受理其他药品生产企业相同品种的一致性评价申请”,是迎难而上还是壮士断腕,是时候做个了断了。
1,国内企业在FDA上市的仿制药品种
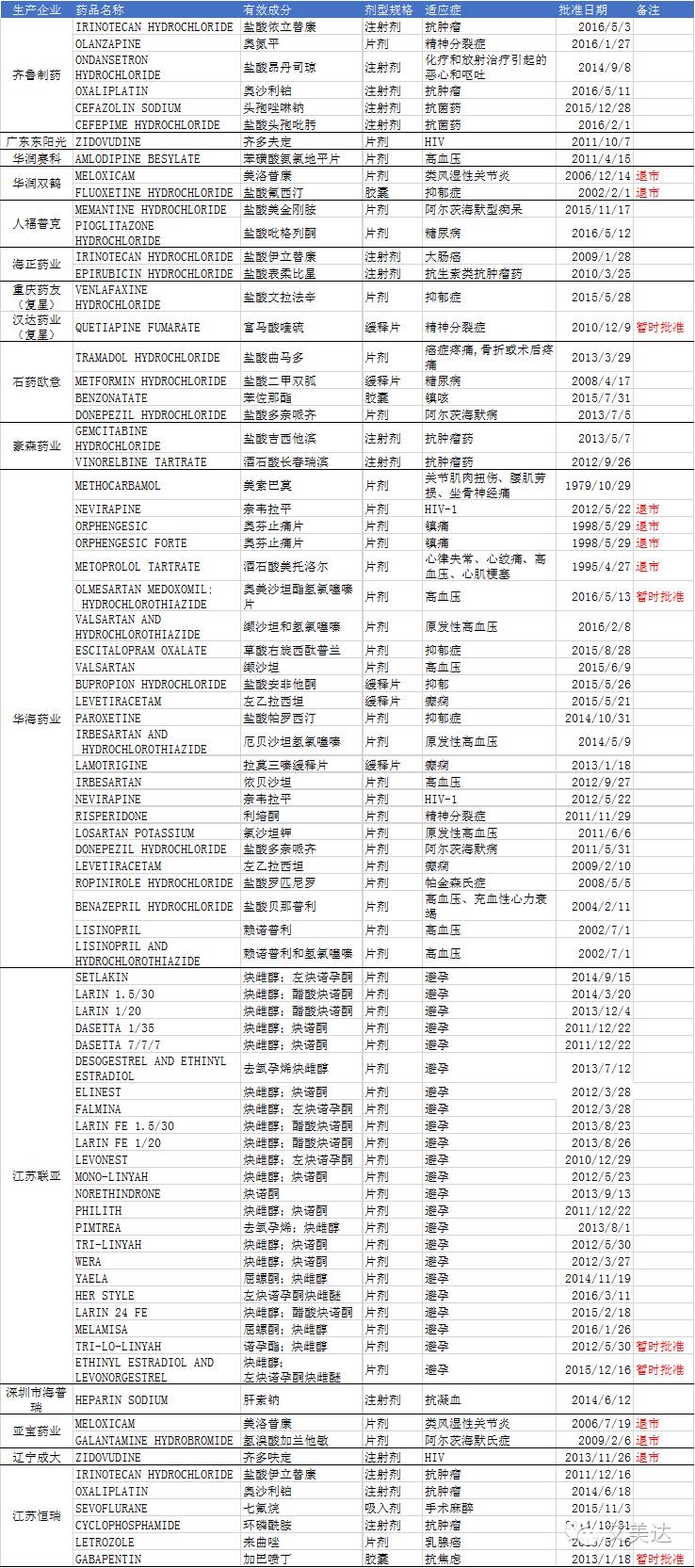
2,申请企业分析(不包含退市品种)
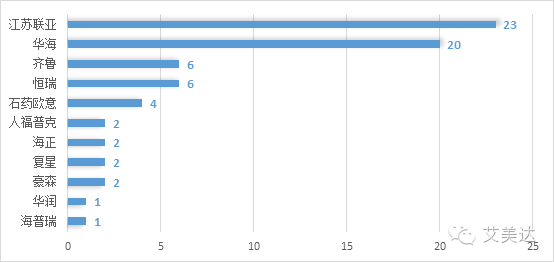
江苏联亚获得批准的品种均为避孕药,由于避孕药规格和包装的特殊性,该企业的品种分析不具有典型性。目前国内仿制药出口美国的前三甲分别是华海药业、齐鲁制药、恒瑞医药。
3,获批时间分析(包含退市品种)
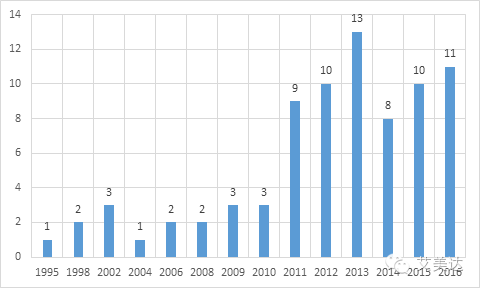
华海、华润从上世纪90年代就已经开始布局美国仿制药市场,国内其它企业随后陆续有品种获批。从2011年开始,我国仿制药出口渐入佳境。
4,获批品种所在治疗领域分析
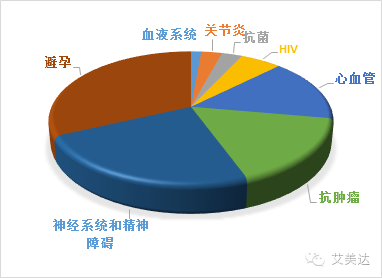
目前,我国获FDA批准的仿制药品种主要集中在神经系统和精神障碍、抗肿瘤以及心血管领域。

