中国小分子靶向药行业研究
里程碑回顾
2001年,诺华的格列卫(Imatinib)获FDA批准用于治疗慢性髓性白血病等疾病,成为全球首个获批上市的小分子靶向药。2005年,阿斯利康的吉非替尼获批进入中国市场,是中国上市的首个小分子靶向创新药。2011年,贝达药业的凯美纳上市,用于治疗晚期肺癌等疾病,是我国第一款自主研发的小分子靶向抗肿瘤药物。自此,中国小分子靶向创新药时代正式拉开帷幕。
产业链概览
小分子靶向药行业主要由三个环节构成,产业链上游包括专利供应商、制药设备供应商、试验耗材供应商和精细化工行业等;中游主要是制药企业;下游是全国各级医疗机构和院内DTP药房。从成本结构来讲,药企小分子靶向药研发支出主要受专利供应商的影响,包括药物结构、晶型、制备方法等专利,成本占比约为70-90%,全球头部供应商包括罗氏、阿斯利康、辉瑞、默沙东和礼来等制药巨头,国内恒瑞、贝达等也开始崭露头角。
市场规模及进展
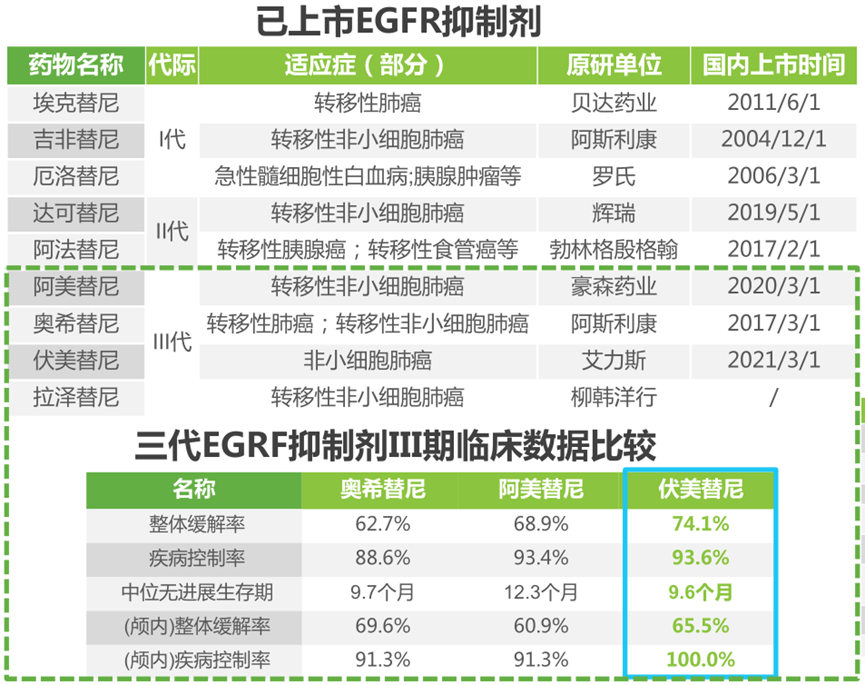
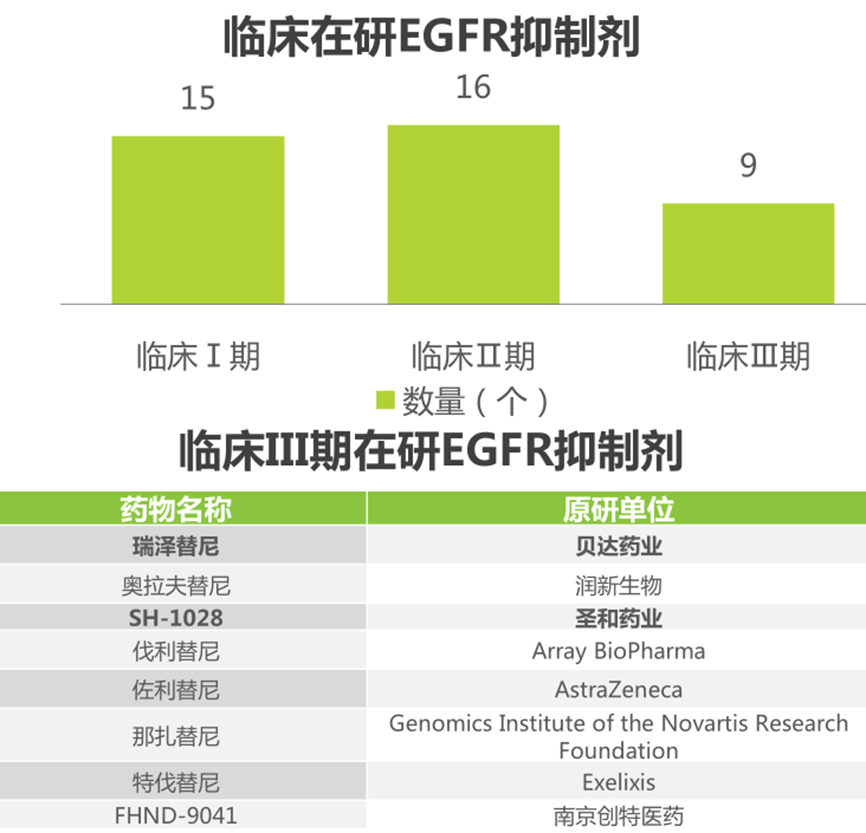
2021年全球小分子创新药市场规模约为1800亿美元,中国市场规模约400亿美元,占全球市场的20%以上。已上市的小分子靶向药可分三类:激酶抑制剂、表观遗传抑制剂和蛋白酶体类抑制剂。激酶抑制剂蛋白激酶的失调与癌症、自身免疫性疾病等具有高度相关性,是最为广泛的疾病治疗靶点。已上市的小分子创新药物中,80%以上是激酶类抑制剂。包括受体酪氨酸激酶抑制剂、受体酪氨酸激酶抑制剂和丝氨酸/色氨酸激酶抑制剂三个类别。EGFR是肺癌最重要的驱动基因之一,在我国非小细胞肺癌(NSCLC)患者中突变阳性率约为40%-50%,靶向EGFR的抗肿瘤药物具有广阔市场。国内有艾力斯于2021年3月上市了三代EGRF抑制剂伏美替尼,治疗效果与前两个三代EGFR抑制剂相比更为显著,成为在国内上市的第三个三代EGFR抑制剂,并于2021年12月进入国家医保名录。临床III期在研的EGFR抑制剂中,贝达药业的泽瑞替尼,圣和药业的SH-128也被寄予厚望。
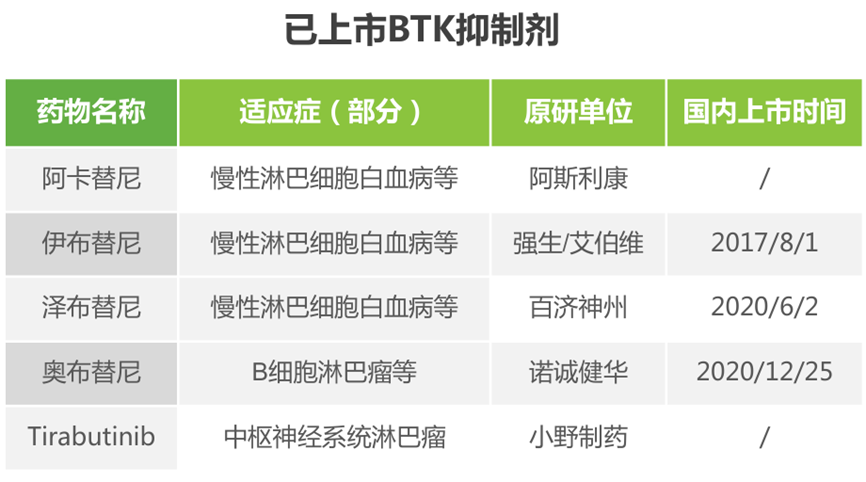
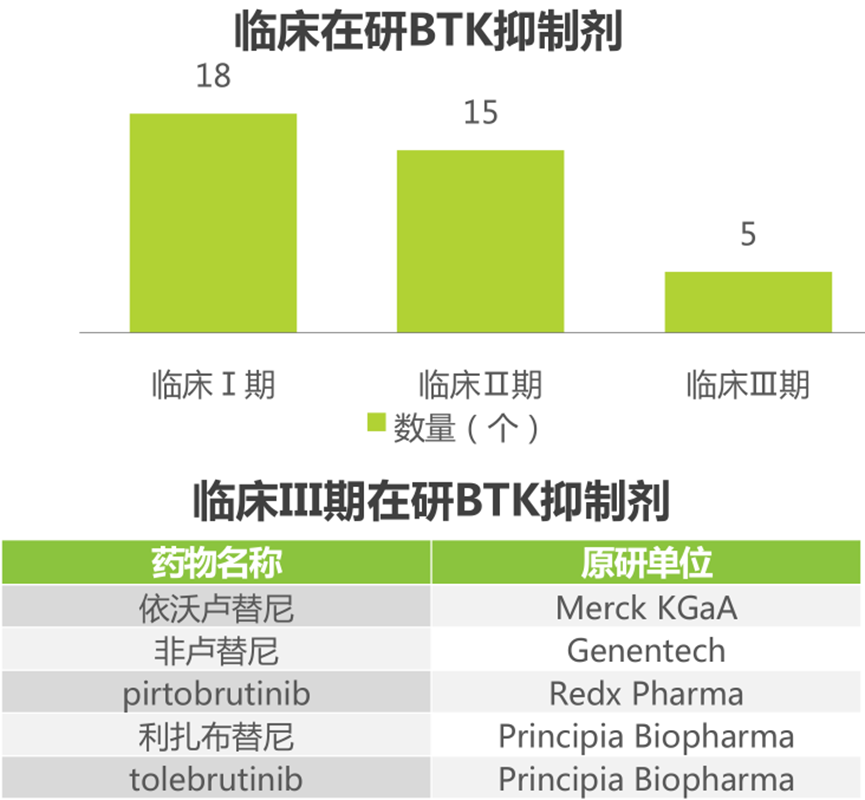
来源于艾瑞咨询BTK(布鲁顿氏酪氨酸激酶)是B细胞受体信号转导通路中的关键激酶,在不同类型恶性血液病中广泛表达,参与B细胞的增殖、分化与凋亡过程。全球首个上市的BTK抑制剂是伊布替尼,用于复发难治的慢性淋巴细胞白血病和套细胞淋巴瘤,2017年获批在中国上市,2018年进入医保名录,2020年全球销售额达到94亿美元以上。百济神州的泽布替尼和恒瑞的阿帕替尼是国内广受关注的BTK抑制剂。泽布替尼是我国第一个在美国获批上市的原研创新药,2020年在美销售额4170万美元;阿帕替尼2014年上市,2017年进入医保,2020年销售额为23.90亿元人民币,目前已有2个适应症获批上市,超过5个联合用药方案/新适应症正在开展III期临床。截至目前,全球还有5个新的BTK抑制剂处于临床III期,但国产原研BTK抑制剂均尚处临床早期阶段。
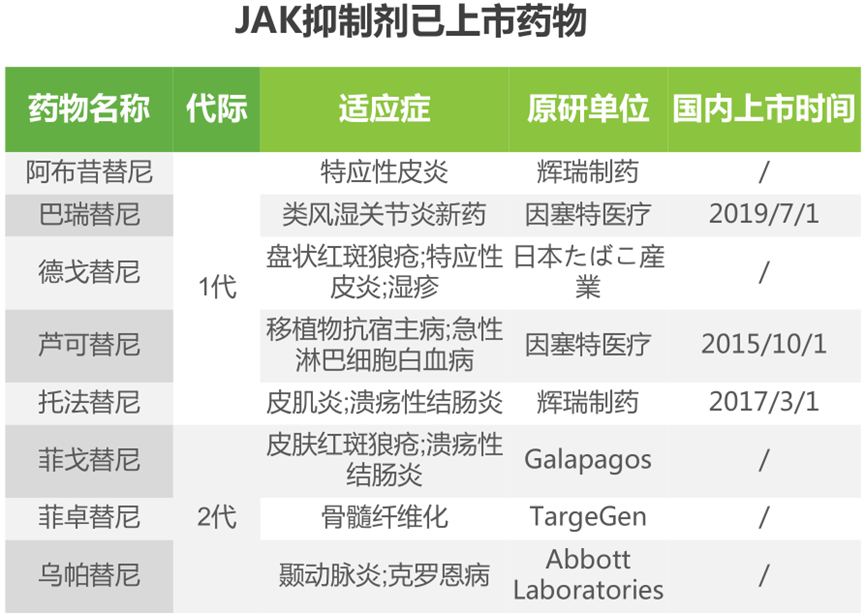
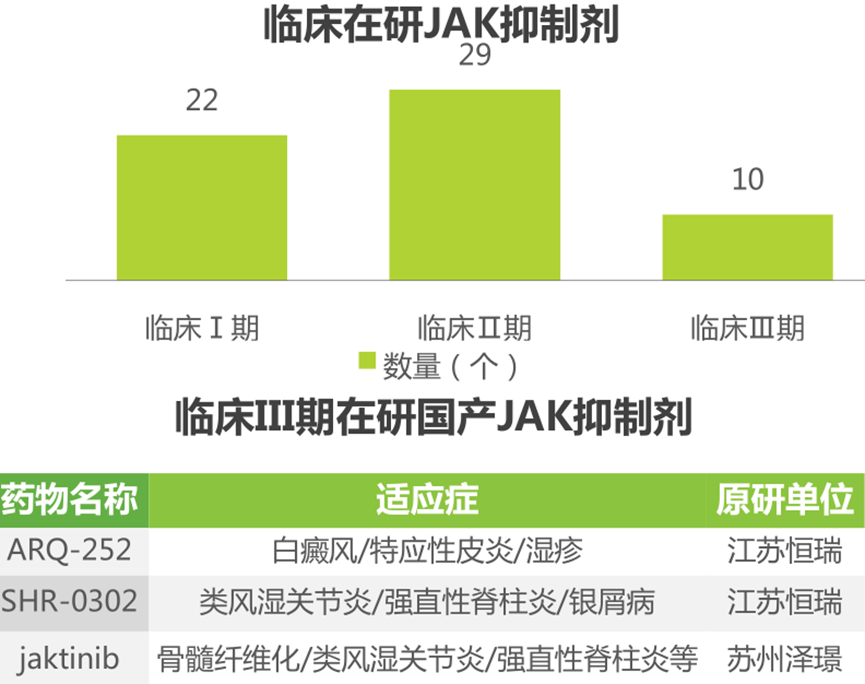
JAK-STAT信号通路是由细胞因子刺激的信号转导通路,参与细胞的增殖、分化、凋亡以及免疫调节等生物学过程。JAK抑制剂可选择性抑制JAK激酶,阻断JAK/STAT通路,临床上主要用于血液系统疾病、肿瘤、类风湿性关节炎及银屑病等疾病治疗。目前全球已经上市8款JAK抑制剂,第一代为芦可替尼、托法替布、巴瑞替尼、培非替尼和迪高替尼;第二代为菲卓替尼、乌帕替尼和非戈替尼。适应症包括类风湿性关节炎、骨髓纤维化、银屑病关节炎、移植物抗宿主病等。国内上市的JAK抑制剂有3款,其中托法替布和巴瑞替布用于治疗类风湿性关节炎,芦可替尼用于治疗中危或高危的骨髓纤维化。托法替布片已有多家仿制药上市。芦可替尼和巴瑞替尼尚无国产仿制药上市。截至目前,全球共有10款JAK抑制剂正在进行III期临床试验,包括三款国产JAK抑制剂。可以预见,未来国内JAK抑制剂市场竞争将趋于激烈。
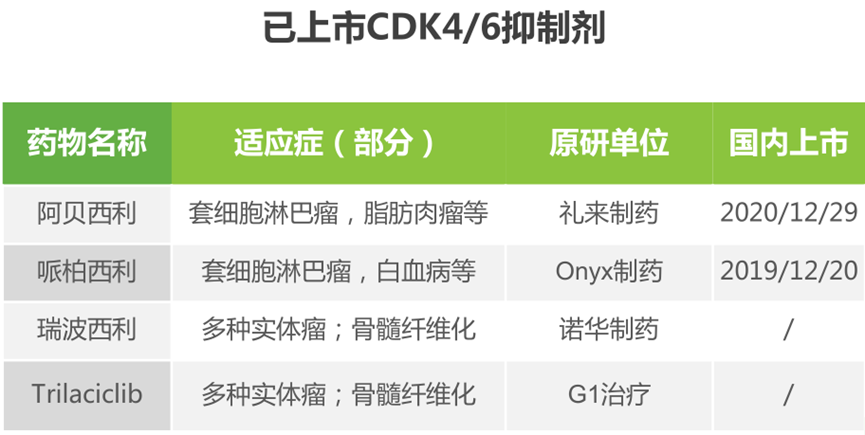
CDK4/6即细胞周期蛋白依赖性激酶4和6,是人体细胞分裂增殖周期的关键条件蛋白,可触发细胞周期从生长期向DNA复制期转变。CDK4/6在很多恶性肿瘤尤其是激素受体(HR)阳性的乳腺癌中过度活跃,表现出显著活性,促使癌细胞增殖扩散,而CDK4/6抑制剂则可将细胞周期阻滞于生长期,从而发挥抑制肿瘤细胞增殖的作用。全球共获批上市四款CDK4/6抑制剂,即辉瑞的哌柏西利、诺华的瑞波西利、礼来的阿贝西利及G1 Therapeutics的Trilaciclib。国内目前已获批上市的CDK4/6抑制剂为哌柏西利和阿贝西利。恒瑞的dalpiciclib的上市申请已被NMPA受理,并进入优先审评通道。截至目前,全球共有三款CDK4/6抑制剂处于临床III期,均为本土原研药物。
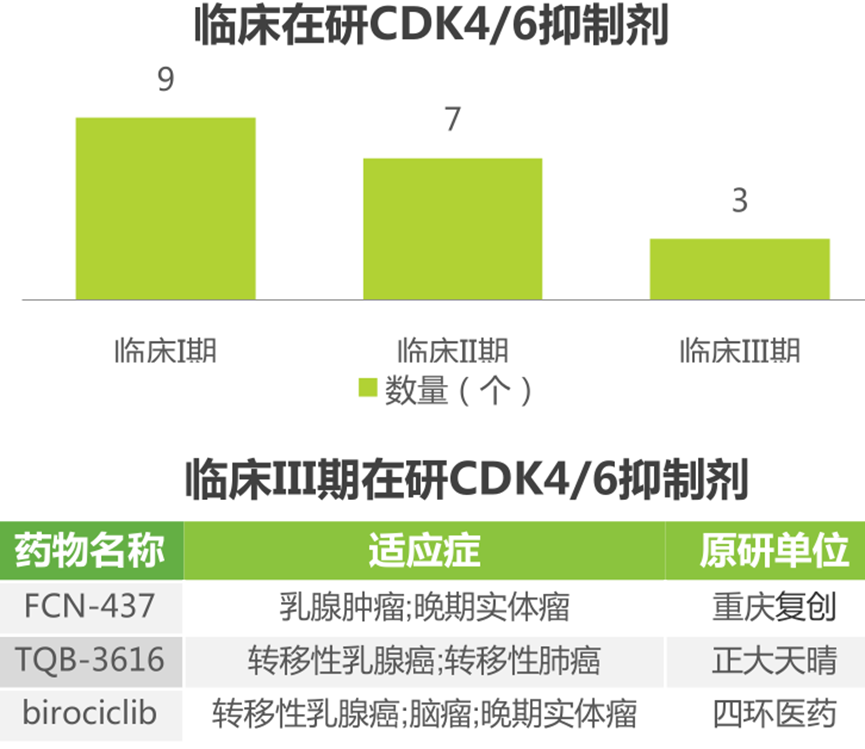
蛋白酶体类抑制剂蛋白酶体是一种大型的多催化酶复合物,在所有真核细胞的细胞核和细胞质中表达,负责人类细胞中超过80%的蛋白质降解。泛素-蛋白酶体系统(UPS)在细胞存活、信号转导、DNA修复和抗原呈递等多个维持细胞蛋白稳态和调节许多生物过程中具有重要作用。UPS的功能障碍与多种人类疾病有关。PARP抑制剂通过抑制肿瘤细胞DNA损伤修复、促进肿瘤细胞发生凋亡,从而增强肿瘤放化疗的疗效,可用于治疗乳腺癌以及卵巢癌、前列腺癌、胰腺癌等拥有相同“流氓基因”的遗传性癌症,被称为对抗各种癌症的“万能武器”。目前,全球获批上市的 PARP 抑制剂有 6 款,分别为阿斯利康的奥拉帕利、Clovis 的鲁卡帕利、葛兰素史克的尼拉帕利、辉瑞的他拉唑帕利、恒瑞医药的氟唑帕利以及百济神州的帕米帕利。国内上市4款,并已全部进入国家医保目录。截至目前,III期临床在研的PARP抑制剂共4款,包括一款以新冠肺炎为适应症的药物。
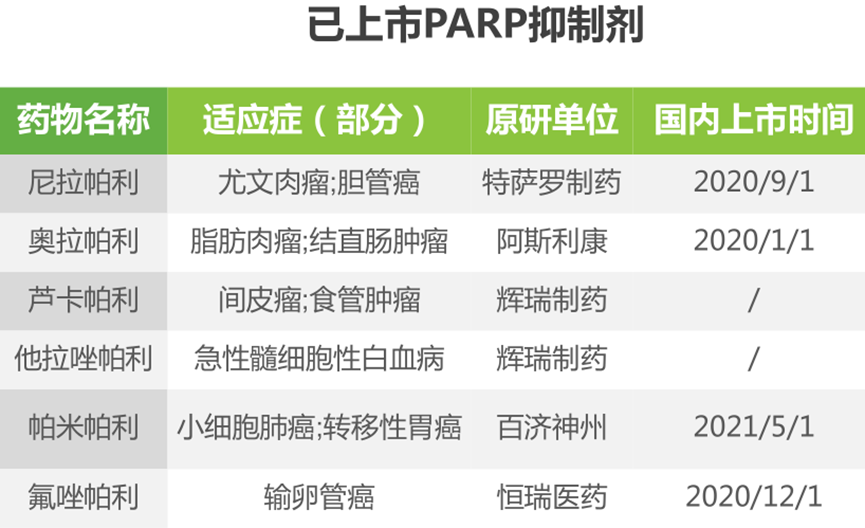
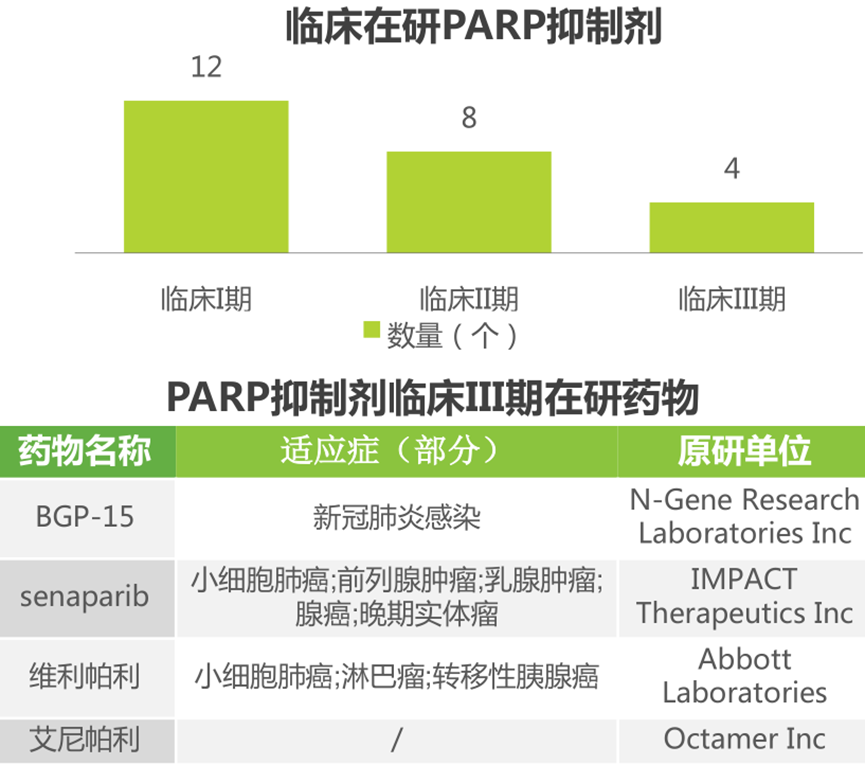
表观遗传抑制剂表观遗传学是遗传学的一个分支学科,研究在不改变基因核苷酸序列的情况下基因表达的遗传变化,受到各种化学修饰酶和识别蛋白的严格调控。异常的表观遗传调控与肿瘤、免疫性疾病和许多罕见疾病等密切相关。虽然许多表观遗传调控蛋白已被确定为潜在的疾病靶点,但目前批准临床使用的表观遗传药物较少,可能是未来小分子创新药研发的方向,潜力靶点包括EZH2,HDAC、IDH1/2等。
开发模式
利用高通量筛选技术获得小分子和靶蛋白的复合晶体结构,并在计算机的辅助下进行结构优化,逐渐成为药物开发的主流。高通量筛选、虚拟筛选、基于结构的药物设计以及基于片段的药物设计逐渐成为小分子药物研发的常见技术。此外,生命科学领域的新突破新技术也为小分子药物研发带来新的研发思路,抗体小分子偶联药物开发已渐成气候,PROTAC 技术、变构调节剂、氘代药物、抗体药物偶联等技术思路也备受期待。
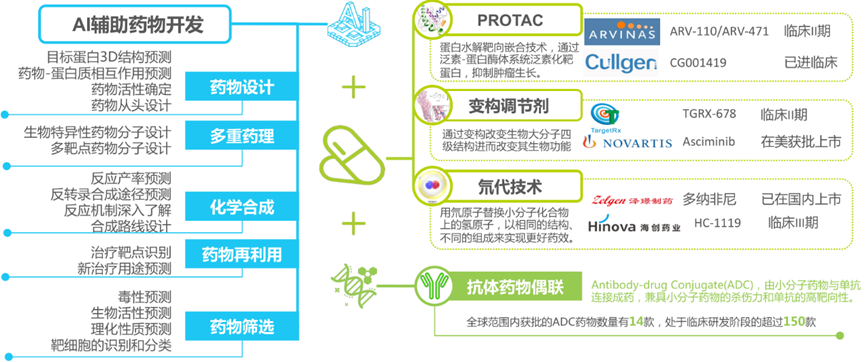
发展痛点

发展趋势
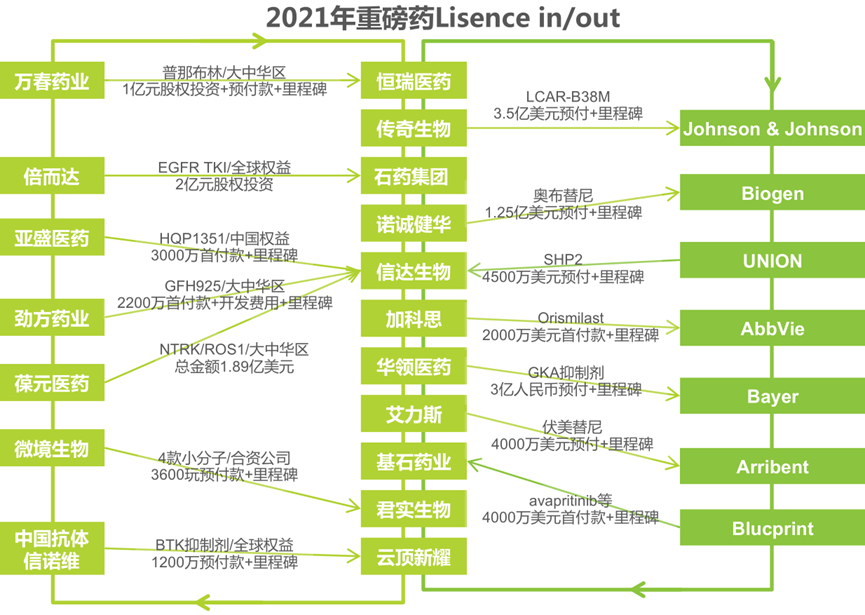
《以临床价值为导向的抗肿瘤药物临床研发指导原则》强调了未来创新药应以临床价值为导向,跟风式内卷不会有未来。持续加码投入研发,FIC/BIC药物的开发能力将成为药企核心竞争力。随着国内外团队进行合作研究越发频繁,国内外技术差距不断缩小,越来越多的企业选择将自己的创新药产品中美同时申报上市,不但有助于打开欧美市场,也代表国产创新药能达到较高认证水平的认可,标志着公司研发实力和临床申报能力达到一定高度。2019年以来,已经有多款国产药物到FDA申报上市,有5款小分子创新药的上市申请获美国FDA受理。同时,国内药企还通过与大型跨国药企之间的权益转让,实现创新药产品布局和收益的最优组合。长远来看,随着研发能力的不断提升,中国创新药的国际化将是个必然趋势,国内将有更多药物实现海外上市。