时评:“有效期与注册证不符”的抗癫痫进口药停了,国内够用?
8月24日,国家药监局对于进口药物左乙拉西坦注射用浓溶液发布公告。暂停进口、销售和使用比利时UCB Pharma S.A.生产的该注射液,商品名为开浦兰,原因则是有部分批次产品标示的有效期与注册批准的有效期不一致。

图源 药监局
这是药监局对于药品境外非现场检查得来的数据,非现场检查,意味着只能通过网络视频等不用亲临生产基地、质检环境中的行为。一般这种检查对于企业而言,相对于直接现场检查的冲击力要低一些。现场检查,有更多的机会去获取一些隐藏信息,所以有些药企会对现场检查非常排斥,甚至不惜用放弃市场来躲避检查。2020年7月,日本一家生产盐酸甲氧那明的原料药企业就做出了书面回应,直接拒绝现场检查。当然中国药监局也没有惯着对方,你不准我去查,那你也别打算来卖,直接暂停进口。

图源 药监局
我们知道药物的用途和稀缺性决定该药品的监管环境,比如以前因亚硝胺杂质而不断被FDA要求整改的华海药业,还有辉瑞等药企。而同样是亚硝胺杂质,另一款糖尿病用药西格列汀则被FDA评估后继续售卖。那么开浦兰的竞品数量,也影响了其后续发展。就这款左乙拉西坦注射用浓溶液而言,在国内有多家企业生产。经查阅,有18个批准文号,且不乏像北京四环制药、扬子江药业、成都倍特药业这样的知名药企,所以说从生产规模上看,不存在稀缺性。从工艺上看,也不具有非常高的壁垒性。
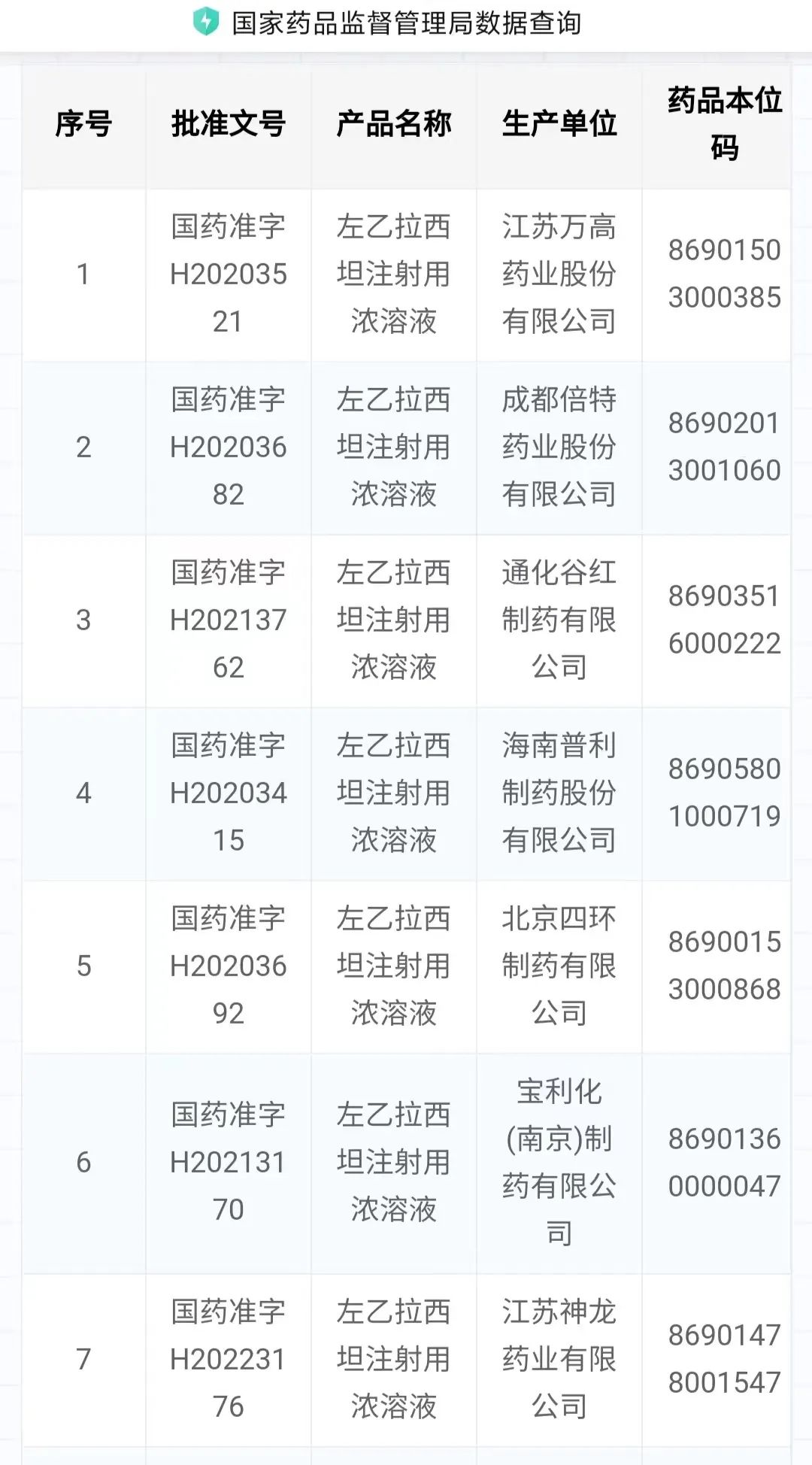
图源 药监局
而影响药品供给关系的,还有原料的因素。如果说多家制剂企业,却只有一个原料药生产企业,那么就有可能遭遇巴曲酶原料药的问题。当年先声药业控制住巴曲酶原料药,最终被罚一亿多人民币。而我们案例中的这款左乙拉西坦注射用浓溶液,则有至少四家原料生产企业。其中包括珠海联邦制药和深圳信立泰药业,所以原料稀缺性问题也不大。
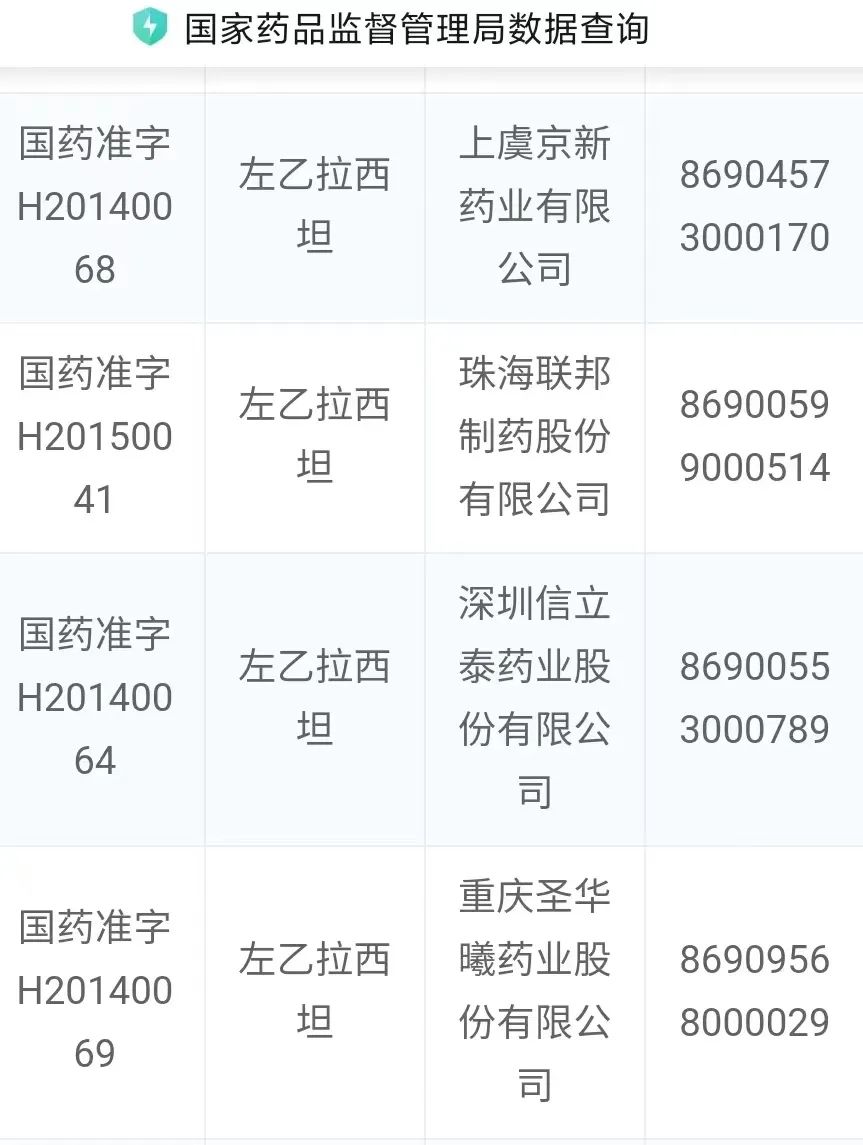
图源 药监局
目前不清楚具体是把有效期改短了还是改长了,从以往案例,比如韩国的火鸡面,就有把进口到中国的有效期延长,以提高货架期,有效期的变动一般与工艺乃至配方有密切关系。火鸡面当时就是改了生产配方,而公告里的开浦兰并没有提到具体细节,我们也只能粗略推断。
不清楚只是标识出错,还是涉及到配方工艺变动,但无论如何,当一个非常明显的错误出现了,那么可能有其他问题伴生,所以药监局对于这次的处理是非常得当的。药品供给关系就是“有中选优”的过程。尤其是国内存在大批竞品的情况下,把握好产品质量,与集采时的定价都显得尤为重要,千万不要让集采时的降价与性能改变挂钩。

